- Es una condición en la que el epitelio escamoso del esofago distal es substituido por epitelio columnar tipo intestinal (metaplasia intestinal especializada). Es el reemplazo del epitelio normal del esófago por células que tienen similitud con el epitelio del intestino delgado.
- 1 al 2% de la población de los Estados Unidos tienen EB. Está relacionado con el aumento de la Obesidad en Estados Unidos
- El EB ocurre en pacientes con o sin síntomas de enfermedad de reflujo. Cerca de la mitad de los pacientes con EB no tienen síntomas de reflujo
- La mayor parte de las veces el EB no se detecta
- Se relaciona con la exposición del esófago a reflujo ácido o biliar
A que pacientes con Enfermedad de Reflujo se debe estudiar: Hombres con Enfermedad de Reflujo > 5 años o con síntomas frecuentes (semanal); pacientes > 50 años; raza blanca; obesos; antecedentes de hábitos tabáquicos; antecedentes familiares de primer grado de EB o Cancer de Esofago
- Tiene un 10% de posibilidades de progresar a adenocarcinoma de esofago. El adenocarcinoma de esofago es el cancer de mayor crecimiento en su incidencia en el hemisferio occidental
- El esófago de Barrett (EB) progresa a adenocarcinoma invasivo a través de los estadios de la metaplasia intestinal (EB no displásico), displasia de bajo grado, displasia de alto grado, carcinoma intramucoso y por último adenocarcinoma.
La progresión de metaplasia, displasia de bajo grado, displasia de alto grado y adenocarcinoma no se cumple de manera secuencial en muchos pacientes. Existe un riesgo aproximado para desarrollar cáncer entre 0.3-0.5% al año
Estudios recientes han demostrado que en la minoría de pacientes el cáncer se desarrolla siguiendo la secuencia tradicional en la cual existen alteraciones genéticas o epigenéticas que inactivan los genes supresores y activan los oncogenes lo cual produce inestabilidad genómica. Pareciera que la mayoria de los pacientes con cáncer presentan una mutación del gen p53. Quiere decir que existen pacientes con cancer en los que no se tienen antecedentes de displasia.
- La endoscopia superior es la herramienta más eficaz para el diagnóstico de esófago de Barrett.
- Para el diagnóstico de esófago de Barrett se requiere endoscopia y biopsia: el endoscopista debe documentar que el epitelio columnar se extiende por encima de la unión gastroesofágica del esófago distal y la biopsia debe demostrar metaplasia intestinal.
- Para diagnosticar el esófago de Barrett la unión escamocolumnar y la unión gastroesofágica deben ser identificadas.
- El esofago de Barrett se puede clasificar como esofago de Barrett corto cuando la distancia entre la línea Z y la unión gastroesofágica es menor a tres centímetros o esófago de Barrett largo cuando la distancia es mayor a 3 centímetros.
A mayor longitud mayor riesgo de malignidad. Por eso el seguimiento depende de la longitud del segmento: Lengüeta de epitelio columnar menor a 1 centímetro: no seguimiento. Esofago de Barrett mayor o igual de 1 centímetro y menor de 3 centímetros: seguimiento cada 5 años. Esofago de Barrett mayor o igual a 3 centímetros y menor de 10 centímetros: 3 años. Extensión máxima mayor o igual a 10 centímetros: referencia a centro especializado. Si el paciente tiene 75 años sin evidencia de displasia no es necesario seguimiento.
- Se puede observar desplazamiento de la unión escamocolumnar proximal en relación a la unión gastroesofágica lo cual es sugestivo de esofago de Barrett.
- La apariencia de la mucosa o la presencia de una línea Z irregular sola o en combinación no son suficientes para el diagnóstico.
- Siempre debe tomarse biopsia para confirmación histológica. Se debe tomar muestras aleatorias en cuatro cuadrantes cada 2 centímetros del segmento de Barrett (Protocolo de Seattle)
En los últimos años se ha demostrado con este esquema de toma de biopsias cerca del 95% del segmento con probable Barrett no se biopsia lo cual limita la eficacia del procedimiento
- La clasificación de Praga se desarrolló para estandarizar la clasificación del esofago de Barrett. En esta clasificación la longitud máxima (M) (incluyendo las lenguetas) del esofago de Barrett y la longitud circunferencial del segmento de Barrett (C) se miden durante el procedimiento endoscópico. El resultado obtenido puede ser utilizado para el seguimiento del Esofago de Barrett. Es un procedimiento validado cuando el segmento de Barrett es mayor a 1 cm.
- La presencia de adenocarcinoma temprano intramucoso o displasia de alto grado no debe llevar a esofagectomia en la actualidad. Existen diferentes técnicas de ablación que permiten el manejo endoscópico de esta patología.
ENDOSCOPIA:
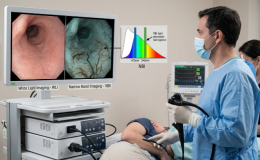
Se debe llevar a cabo con endoscopios de alta resolución y luz blanca, con capacidad de realizar cromoendoscopia óptica.
Algunas de las ventajas específicas de la cromoendoscopia óptica en el diagnóstico del esófago de Barrett son:
- Realce de detalles y características del tejido: La cromoendoscopia óptica permite resaltar detalles microscópicos y características sutiles del tejido esofágico, lo que ayuda a identificar áreas de metaplasia intestinal y otras anomalías con mayor precisión.
- Diferenciación de tejidos: Los filtros de luz utilizados en la cromoendoscopia óptica pueden ayudar a diferenciar entre el tejido normal y el tejido con metaplasia intestinal o displasia, que son hallazgos asociados con el esófago de Barrett.
- Evaluación de la extensión y el grado de afectación: La cromoendoscopia óptica permite una evaluación más completa de la extensión del esófago de Barrett y el grado de afectación del tejido. Esto es importante para planificar el tratamiento y el seguimiento adecuado.
- Guiado para la toma de biopsias dirigidas: Con la cromoendoscopia óptica, los médicos pueden identificar áreas sospechosas y realizar biopsias dirigidas a esas zonas específicas. Esto aumenta la probabilidad de obtener muestras representativas para su análisis en el laboratorio y ayuda a confirmar el diagnóstico de esófago de Barrett.
- Mejora en la detección temprana de lesiones precancerosas: La cromoendoscopia óptica puede ayudar a detectar lesiones precancerosas en estadios tempranos, lo que permite un tratamiento oportuno y eficaz y mejora las perspectivas de los pacientes.
Los estudios que comparan NBI/FICE/I-scan con cromoscopia han demostrado que tienen tasas similares para la detección de neoplasia. La mayoría de lesiones neoplásicas tempranas pueden ser vistas con luz blanca y alta definición.
- El EB se diagnostica cuando existe una extensión de mucosa asalmonada en el esofago proximal que se extiende > 1 centimetro por encima de la unión gastroesofágica con biopsia confirmatoria de metaplasia intestinal
- La biopsia no se debe realizar en presencia de una línea Z normal o la línea Z < 1 centímetro.
- En presencia de EB el endoscopista debe describir la extensión del cambio metaplásico incluyendo la longitud circunferencial y segmentaria utilizando la Clasificación de Praga.
- Se debe reportar la localización del hiato diafragmático, unión EG y unión escamocolumnar.
- En pacientes con sospecha de EB al menos 8 biopsias aleatorias deben ser obtenidas para maximizar la histología. En pacientes con segmento corto (1-2 centímetros) en la cual es difícil obtener las 8 muestras se deben tomar al menos 4 muestras circunferenciales y una biopsia por lengüeta de EB. Las lesiones sospechosas deben ser biopsiadas y enviadas en frasco separado.
- En pacientes con sospecha de EB sin metaplasia intestinal se debe repetir la endoscopia en 1-2 años para descartar EB.
Al momento de la endoscopia no se debe sobre insuflar porque se sobre diagnostica esta patología
Para documentar que el epitelio columnar compromete el esófago el endoscopista debe identificar la unión escamocolumnar y la unión gastroesofágica. El epitelio columnar tiene un color asalmonado mientras que el epitelio escamoso tiene un color pálido. La yuxtaposición de ambos constituye la unión escamocolumnar o línea Z, la unión gastroesofágica se reconoce endoscópicamente como la extensión proximal de los pliegues gástricos. Cuando la unión escamocolumnar y la unión gastroesofágica coinciden se concluye que todo el esofago esta cubierto por epitelio escamoso. Si la biopsia demuestra metaplasia intestinal se confirma el diagnóstico de esófago de Barrett.
Lo primero es determinar la posición real de la union esofagogastrica que es a nivel del límite proximal de los pliegues gástricos (Origen: 0 cms). Luego determinar la extensión circunferencial de la metaplasia (C:2.0 cms). Si existe prolongación proximal se determina la extensión máxima de la metaplasia (M:5.0 cms)
Se debe documentar: Clasificación de los Ángeles para Esofagitis por Reflujo, Clasificación de Praga para esofago de Barrett y Clasificación de Paris para determinar el tipo de lesión
Clasificación de Los Angeles para Esofagitis por Reflujo:
La clasificación de Los Ángeles es una herramienta útil en el diagnóstico y seguimiento del esófago de Barrett y otras condiciones relacionadas con el reflujo gastroesofágico (ERGE).

Clasificación de Praga:
La clasificación de Praga divide el esófago de Barrett en segmentos y proporciona una descripción sistemática de las características endoscópicas encontradas en cada segmento. Esta clasificación es útil para estandarizar la comunicación y el seguimiento de los pacientes con esófago de Barrett.
El sistema de clasificación de Praga se basa en cuatro características principales:
- Longitud del segmento de Barrett: El esófago de Barrett se divide en segmentos longitudinales y se mide la extensión del tejido columnar metaplásico en cada segmento.
- Circunferencia de la afectación: Se describe la circunferencia del esófago de Barrett en cada segmento, que puede ser segmentaria (menos del 50% de la circunferencia) o circunferencial (50% o más de la circunferencia).
- Presencia de displasia: Se evalúa la presencia de displasia, que es un cambio en las células que puede indicar un mayor riesgo de cáncer. La displasia se clasifica en tres categorías: negativa para displasia, displasia de bajo grado y displasia de alto grado.
- Presencia de cáncer: Se registra si se encuentra cáncer en el esófago de Barrett.

Criterios de Seattle para la toma de Biopsias:
- Lo primero es observar con luz blanca, endoscopio de alta definición y cromoendoscopia. Buscar cualquier cambio de patrón, áreas de neovascularización, nódulos, depresiones, etc.
- Se recomienda inspeccionar cada segmento de 1 centímetro por 1 minuto.
- Hacer énfasis en la pared derecha y el segmento proximal (en especial en segmentos largos).
- Utilizar capuchón.
- Hacer énfasis en la región más proximal porque allí puede existir displasia.
- Se debe tomar biopsias en los 4 cuadrantes cada 1-2 centímetros (consume demasiado tiempo).
- La adherencia al protocolo de Seattle es baja.
- A pesar de usar este protocolo entre el 94-96% de la mucosa no se analiza
- El análisis histopatológico debe ser hecho por un patólogo con experiencia en EG.

Consideraciones para el Screening:
- No tomar biopsias de una línea Z irregular
- Diferir biopsias se existe esofagitis erosiva
- La presencia de displasia de bajo grado debe ser confirmada y revisada por el mismo u otro patólogo, si no se encuentra displasia puede ser tratada como no displasia, si se confirma displasia de bajo grado repetir endoscopia en 3-6 meses con inhibidores de bomba de protones, posible resección de lesiones sospechosas si son visibles.
- Se considera tomar muestras de la unión esófago gástrica (es sitio frecuente de recurrencias).
Según la Esge 2017 se recomienda el siguiente es que de seguimiento en EB sin displasia: 1-3 centímetros: 5 años. 3-10 centimetros: 3 años > 10 centímetros: referir a centro especializado ya que se considera que tiene displasia de bajo grado.
Existen otros proyectos para mejorar la detección endoscópica de la patología en la actualidad:
Existe un procedimiento que permite obtener muestras grandes de áreas específicas de la mucosa en busca de áreas de displasia de bajo y alto grado de EB: WATS3D
El WATS3D permite obtener muestras transepiteliales de áreas sospechosas de EB para su posterior análisis con software e inteligencia artificial. Es un procedimiento sencillo y efectivo.
Error frecuente:
No tomar suficiente tiempo para limpiar e inspeccionar la mucosa. Si no se limpia bien es imposible la detección de lesiones más pequeñas en el EB. Se sugiere emplear unos cuantos minutos para optimizar la imagen de manera que se incrementa la posibilidad de detectar la enfermedad. Se puede utilizar waterjet para limpiar el segmento de Barrett (1-2 minutos), para determinar si se ha logrado una buena limpieza se pasa a cromoscopia óptica y NBI. Se sugiere emplear entre 3-5 minutos utilizando la luz blanca alternando con la cromoscopia óptica para tener otra perspectiva. Se debe realizar retroversión para inspeccionar la zona de peligro que es donde el EB se introduce en la hernia hiatal. Esta es un áreas con riesgo elevado de neoplasia que puede no ser bien inspeccionada con el endoscopio. Hay que saber como es el aspecto de la neoplasia en el EB
Ver más, biopsiar menos
Link sugerido: www.best-academia.eu
Saber dónde mirar:
Generalmente las lesiones se ubican del lado derecho de la pantalla.
Métodos diagnósticos actuales:
Algunas modalidades de imagen han sido aprobadas y se encuentran disponibles en la actualidad.
Debido a que la displasia no tiene características macroscópicas definidas se toman muestras aleatorias lo cual aumenta el error al momento de la detección de la patología. Cuando se detecta displasia de alto grado uno de cada tres pacientes tiene cáncer invasivo por lo tanto, la toma de múltiples biopsias disminuye el problema pero no lo resuelve.
Links sugeridos:
Early Detection of Esophageal Cancer and Barrett’s Esophagus: Recent Advances
Luz blanca con endoscopia de alta definición:
El EB se sospecha cuando en la endoscopia se detecta mucosa asalmonada en el esófago distal. Las guías actuales tienen como requisito la toma de biopsias para documentar la metaplasia intestinal y diferenciar las forma fúndica o cardial de la metaplasia gástrica. Más allá del diagnóstico inicial el seguimiento utilizando resolución estándar con luz blanca no es confiable para la visualización de displasia o neoplasia temprana. Se depende por lo tanto de la toma de biopsia. El video endoscopio utiliza un circuito eléctrico integrado hecho de semiconductores fotosensibles (CCD), los aparatos de video estándar tienen entre 100000 y 300000 pixeles y la resolución de la imagen varía en cuanto a la capacidad de discriminación entre 2 puntos adyacentes (distancia focal entre 1-9 centímetros) más allá de este rango las imágenes aparecen desenfocadas. Existen endoscopios de alta resolución entre 600000-1000000 de pixeles por CCD que son capaces de producir imágenes de alta definición con posibilidad de detección de anormalidades microscópicas en las estructuras glandulares y vasculares ( permiten el examen detallado en un rango menor a 3 mm).
La endoscopia de alta definición mejorar la detección de áreas de displasia en comparación con la endoscopia convencional con luz blanca.

Narrow Band Imaging:
El Narrow band imaging (NBI) es la técnica mejor estudiada en la actualidad para detectar la displasia en EB. Se puede visualizar cambios tempranos en la angiogénesis (aumento de la densidad de la microvasculatura) asociados al desarrollo de displasia y neoplasia superficial. Utilizando filtros de luz, la contribución de la luz azul aumenta al modificar el ancho de banda del componente rojo,verde y azul, reduciendo los verdes y eliminando la luz roja, Esto resulta en una banda estrecha constituida por luz azul-verde que mejora la visualización de los patrones mucosos. La luz azul se absorbe por la hemoglobina para la detección de patrones glandulares mucosos, patrones vasculares y la presencia de vasos anormales relacionados con displasia.

Links sugeridos:
NBI and update in Barrett Esophagus. Dr Prateek Shanna
Cromoendoscopia con azul de Metileno:
Es laborioso y poco práctico utilizar endoscopia de alta resolución y magnificación sobre superficies mucosas extensas. Por lo tanto se puede combinar con cromoendoscopia con la finalidad de detectar anormalidades mucosas. Se utilizan varias sustancias como el Lugol, azul de metileno, índigo carmín y ácido acético para la detección de metaplasia intestinal especializada. El Lugol se ha utilizado para mejorar la detección del carcinoma epidermoide y displasia del tracto gastrointestinal debido a su absorción por parte de las células que contienen glucógeno. El Lugol se utiliza en pacientes con riesgo incrementado de cáncer epidermoide (fumadores, alcoholismo e ingestión de lejía). El azul de metileno se utiliza para la detección de Esofago de Barrett por lo que es absorbido por el epitelio intestinal y no por el epitelio epidermoide o gástrico. El azul de metileno, índigo carmín y ácido acético combinados con endoscopia de magnificación identifica los patrones glandulares mucosos. Guelrud y colaboradores han identificado cuatro patrones utilizando ácido acético y endoscopia de magnificación asociados a metaplasia intestinal. existe controversia en cuanto al daño de ADN con el azul de metileno y luz blanca, hallazgos similares se han encontrado con el uso de ácido acético que puede alterar la estructura celular proteica.
Ácido Acético:
El estudio ABBA ha demostrado que aplicar ácido acético mejora significativamente la detección de displasia en comparación con el protocolo de Seattle.
Autofluorescencia:
La autofluorescencia es una técnica que diferencia los tipos de tejido basado en la diferencia en la emisión de fluorescencia. Cuando los tejidos se exponen a luz de onda corta, las sustancias biológicas emiten luz fluorescente con luz de onda larga (autofluorescencia). Las moléculas responsables de la auto fluorescencia incluyen el colágeno, la elastina, flavina, porfirinas y aminoácidos aromáticos (todos con características propias de emisión espectral). La autofluorescencia detecta diferencias entre la fluorescencia endógena normal, displasia y neoplasia utilizando luz azul que se detecta con lentes de alta definición. La mucosa normal (color verde) y la mucosa con displasia o neoplasia (color rojo o púrpura). Su efectividad puede mejorar cuando se combina con NBI.
Endomicroscopia confocal con láser:
La microscopia confocal es una técnica avanzada de imagen que se utiliza en el estudio del esófago de Barrett y otras afecciones del tracto gastrointestinal. Esta técnica permite obtener imágenes detalladas de las células y tejidos en tiempo real, a nivel microscópico, sin la necesidad de tomar muestras de tejido (biopsias). Es una herramienta valiosa para obtener información más precisa y detallada sobre la estructura y las características del tejido esofágico.
Algunas de las principales ventajas son las siguientes:
- Evaluación en tiempo real: La microscopía confocal con láser permite al médico visualizar en tiempo real las células y estructuras del tejido esofágico sin la necesidad de tomar biopsias. Esto proporciona información instantánea y detallada sobre el estado del tejido, lo que puede ser especialmente útil durante una endoscopia para guiar el diagnóstico y tomar decisiones en el momento.
- Alta resolución y detalle: La microscopía confocal con láser ofrece una alta resolución y capacidad de ampliación, lo que permite a los médicos examinar las células y tejidos a nivel microscópico con gran detalle. Esto facilita la detección de cambios celulares sutiles y anormales asociados con el esófago de Barrett.
- Toma de imágenes no invasiva: A diferencia de la biopsia, la microscopía confocal con láser es una técnica no invasiva que no requiere la extracción de muestras de tejido. Esto significa que no se necesitan procedimientos adicionales para obtener información detallada del tejido, lo que puede reducir la incomodidad y el riesgo de complicaciones.
- Guía para biopsias dirigidas: La microscopía confocal con láser puede ayudar a identificar áreas anormales o sospechosas en el esófago. Esto permite que los médicos realicen biopsias dirigidas a esas zonas específicas, lo que aumenta la probabilidad de obtener muestras representativas y precisas para su análisis en el laboratorio.
- Reducción del tiempo y costos: Al proporcionar información en tiempo real, la microscopia confocal con láser puede reducir la necesidad de realizar múltiples procedimientos y pruebas, lo que puede ahorrar tiempo y costos tanto para los pacientes como para los sistemas de salud.
Links sugeridos:
Opciones avanzadas de imagen para Esofago de Barrett (Mayo Clinic)
Tomografía de coherencia óptica:
Endomicroscopia láser volumétrica:
Espectroscopia:
Algoritmo por Computadora:
El uso de inteligencia artificial (IA) en el diagnóstico del esófago de Barrett ofrece varias ventajas significativas que pueden mejorar la precisión y eficiencia del proceso de diagnóstico. Algunas de las ventajas clave incluyen:
- Detección temprana: La IA puede ayudar a identificar de manera temprana y precisa signos de esófago de Barrett, incluso en sus etapas iniciales, lo que permite un tratamiento oportuno y evita la progresión de la enfermedad a etapas más avanzadas.
- Mayor precisión en la interpretación de imágenes: La IA puede analizar grandes cantidades de imágenes endoscópicas y de otros estudios para detectar patrones y características sutiles que los médicos pueden pasar por alto o pueden ser difíciles de percibir a simple vista.
- Reducción de errores y sesgos: La IA puede ayudar a reducir los errores y sesgos humanos en la interpretación de los resultados, ya que su enfoque es puramente basado en datos y no se ve influenciado por factores subjetivos.
- Aumento de la eficiencia: La IA puede agilizar el proceso de diagnóstico al analizar rápidamente grandes cantidades de datos y ofrecer resultados en tiempo real, lo que permite a los médicos tomar decisiones más informadas y acelerar el inicio del tratamiento.
- Integración con otros datos clínicos: La IA puede combinar y analizar datos de diferentes fuentes, como imágenes endoscópicas, historias clínicas, resultados de biopsias y otros estudios, para proporcionar un diagnóstico más completo y holístico.
- Personalización del tratamiento: La IA puede ayudar a identificar patrones y características específicas del esófago de Barrett en pacientes individuales, lo que permite una personalización más precisa del tratamiento según las necesidades y características de cada persona.
- Investigación y desarrollo: La IA puede acelerar la investigación en el campo del esófago de Barrett, permitiendo el análisis de grandes bases de datos y la identificación de nuevas asociaciones y tendencias que podrían llevar a avances en el diagnóstico y tratamiento.
Biomarcadores
TissueCypher:
Manejo del Esofago de Barrett:
- Toda lesión visible independientemente del grado de displasia debe ser resecada. La biopsia dicta la conducta a seguir.
- El tratamiento endoscópico es de primera elección para el adenocarcinoma precoz y el EB displásico
- La resección mucosal endoscópica es el tratamiento de elección para cualquier lesión visible
Algoritmo:
- Sin displasia: la ablación es una opción, pero su papel es controversial
- Displasia de bajo grado: considerar ablación si es multifocal, lesión nodular, historia familiar, histopatología confusa
- Enfermedad nodular: tratar de acuerdo a biopsia obtenida de la resección mucosal endoscópica; sin cancer, cancer en la mucosa o SM1 realizar ablación; mayor a SM1 realizar radioterapia y esofagectomia
- Displasia de alto grado en superficie plana: ablación
El peor error es hacer ablación sobre mucosa nodular
A quién tratar:
- EB sin displasia: Endoscopia control en 3-5 años
- EB con diagnóstico de displasia no definitivo: tratar de forma similar como displasia de bajo grado
- EB con displasia de bajo grado: Terapia de erradicación endoscópica. El tratamiento disminuye el riesgo de progresión a displasia de alto grado hasta un 25% y 7.5% a cáncer. Es un diagnóstico difícil que debe ser confirmado por un segundo patólogo, se recomienda control a los 6 meses.
- EB con displasia de alto grado: Terapia de erradicación endoscópica.
- Adenocarcinoma intramucoso T1a: Terapia de erradicación endoscópica.
- Adenocarcinoma submucoso T1b: Terapia de erradicación endoscópica si: la invasión submucosa < 500 um, ausencia de invasión vascular, tumor bien diferenciado y borde de resección libre.
La presencia de mucosa esofágica elevada,irregular o nodular esta asociada a malignidad por lo que se indica resección mucosal o submucosal endoscópica. Si posterior a la resección muestra displasia de bajo grado, displasia de alto grado o T1a sin compromiso linfático o vascular se aplica terapia ablativa posterior.
A quien no tratar:
- Lesiones profundas: toda lesión SM1 o más profunda es candidata a esofagectomia, toda lesion SM1 se puede manejar endoscopicamente si el paciente no es candidato a cirugía
- Lesiones agresivas: pobremente diferenciadas, invasión linfovascular
- Lesiones muy grandes
Tratamiento del cancer de esofago T1b:
- El tratamiento endoscopico de cualquier cancer en esofago depende de la profundidad de la invasión y de la presencia de adenopatías.
- El riesgo de presencia de adenopatías en cáncer T1 es menor al 1%, en caso de tumores submucosos el riesgo de adenopatías aumenta entre 0-46%.
- Tenemos pacientes con T1b con bajo riesgo: sm1 (invasión a la submucosa < 500 ug,cáncer bien diferenciado, sin invasión linfo-vascular, resección radical R0)

Terapias disponibles para Esofago de Barrett:
Terapias de resección: Resección mucosal endoscópica. Disección submucosal endoscópica.
Terapias de Ablación: Radiofrecuencia. Terapia Híbrida con Argón Plasma. Crioterapia. Balón para Crioterapia.
- La inspección es critica: luz blanca con endoscopia de alta definición (cromoendoscopia óptica, capuchón)
- El ultrasonido endoscópico tiene utilidad limitada para el estadiaje T ( se usa para descartar la presencia de adenopatías locales).
- Se debe eliminar todo el segmento.
- El control del reflujo es crítico para evitar recaídas.
Cualquier lesión visible debe ser resecada previo a terapia de ablación
Esofago de Barrett Nodular:
- Resección mucosal Endoscópica:
Existen dos métodos para la resección mucosal endoscópica (RME): la RME con capuchón que consiste en aspirar la lesión que previamente ha sido infiltrada en la submucosa para resecarla. Con este procedimiento se obtiene un fragmento grande, existen varios tamaños de capuchón y requiere experiencia, tiene riesgo de perforación por lo que siempre se recomienda elevar la lesión. La otra posibilidad es la resección con el uso de ligas (mucosectomía con bandas) que es segura, mas rapida y tiene menos complicaciones.
A quién realizar RME: cualquier lesión focal ya sea elevada, plana o deprimida. Si es una lesión deprimida tratar de elevarla. Lesiones < 20 mm requieren resección en bloque. Es muy difícil resecar la muscularis propia
- Disección submucosal Endoscópica
Esofago de Barrett sin Nodulos:
Ablación Térmica:
Las terapias de ablación se comenzaron a realizar con Laser y terapia fotodinámica en la década de los noventa.
Al principio la ablación era un proceso esotérico realizado en centros de referencia terciarios.
Con la llegada de la tecnología se hace ablación a pacientes con displasia de alto grado, displasia de bajo grado, sin displasia y a todo lo que termina en Barrett…
Las guías de tratamiento actuales no recomiendan ablación en pacientes sin displasia
Displasia de Bajo Grado:
Las guías de manejo actuales coinciden en que debe existir una segunda confirmación en pacientes con displasia de bajo grado:

La presencia de nodularidad y focos multifocales de displasia de bajo grado son factores de riesgo para la progresión del EB:
Terapia con Radiofrecuencia:
- Es una técnica efectiva y segura para pacientes con EB con displasia de bajo o alto grado. La resección endoscópica ha demostrado ser una técnica duradera y efectiva con pacientes con displasia de alto grado o adenocarcinoma superficial pero se asocia a mayor grado de estenosis cuando se compara con radiofrecuencia.
- El sistema bipolar produce un campo eléctrico que produce calentamiento del agua intracelular con la evaporación y coagulación de las proteínas y daño celular irreversible. Es similar a calentar un perro caliente en un microondas..
- Se ha demostrado que este procedimiento erradica la displasia y reduce la progresión a cáncer
- Las desventajas son el costo y el efecto destructivo sobre el tejido. El tejido es destruido durante el procedimiento por lo que no se puede analizar a posteriori. Otra desventaja de la radiofrecuencia es que requiere entre 2 a 4 sesiones de tratamiento por un periodo de 3 a 6 meses para erradicar la displasia o el cáncer.
- La eficacia de la radiofrecuencia en términos de erradicación completa de displasia varía entre 90-95%.
- La complicación más frecuente de la radiofrecuencia es la estenosis (5%)
El tratamiento con Radiofrecuencia puede tomar entre 6 y 8 meses de duración

La recurrencia posterior al procedimiento es uno de los temas mas controversiales. Algunos trabajos señalan que la displasia puede recurrir en el 2% por año.
Se recomienda endoscopia en el caso de displasia de alto grado cada 3 meses por 1 año, luego 1 endoscopia anual. Para displasia de bajo grado cada 6-12 meses y luego cada 3 años.
LINKS RECOMENDADOS:
NEJM Procedure: Radiofrequency Ablation in Barrett’s Esophagus with Dysplasia
Radiofrequency Ablation (RFA) Therapy for Treating Barrett’s Esophagus
Circumferential Radiofrequency Ablation of a Long-Segment Barrett’s Esophagus / HALO 360 System
Coagulación híbrida con Argón Plasma:
- El argón plasma es la técnica más disponible para la ablación del EB.
- Es una alternativa para el tratamiento del EB residual y es efectiva para reducir las recurrencias.
- Complicaciones: estenosis (9% de los pacientes)
- Procedimiento: inyección de solución fisiológica al 0.9% con o sin epinefrina) antes de utilizar el AP.
Links recomendados:
Barrett Esophagus – Hybrid APC
Electrocoagulación multipolar:
Ablación con Láser:
Ablación Fotoquímica:
Terapia Fotodinámica:
Ablación con Crioterapia:
La crioterapia es tratamiento de elección en pacientes con EB que no ha respondido a terapia con ablación con radiofrecuencia, pacientes no candidatos a cirugía y pacientes con esofago tortuoso.
Se utiliza la crioterapia con nitrógeno líquido:
- Frío intenso (-196 grados centígrados) con un catéter diseñado para tal fin y con visión endoscopica para congelar el tejido
- Se produce una transferencia de energía rápida y eficiente
- Se calienta y enfría el tejido para obtener el efecto deseado
- No requiere una superficie plana para tratar
- Se puede utilizar el endoscopia en retroflexion
- Existe la opción de utilizar el Crio-balon con óxido nitroso
Screening para el Esofago De Barrett:
Factores de riesgo para el desarrollo de Adenocarcinoma en el esofago de Barrett:
El esófago de Barrett es una condición que aumenta el riesgo de desarrollar adenocarcinoma de esófago, un tipo de cáncer que se origina en el revestimiento del esófago. Algunos de los factores de riesgo que se han identificado para el desarrollo de neoplasia en el esófago de Barrett son:
- Edad: El riesgo de desarrollar cáncer de esófago aumenta con la edad.
- Sexo: Los hombres tienen un mayor riesgo de desarrollar cáncer de esófago que las mujeres.
- Duración de la enfermedad: La duración del esófago de Barrett aumenta el riesgo de desarrollar cáncer de esófago.
- Presencia de displasia: La presencia de displasia en las biopsias de seguimiento es un predictor importante de un mayor riesgo de cáncer de esófago.
- Longitud del segmento de Barrett: El riesgo de cáncer de esófago aumenta con la longitud del segmento de Barrett.
- Reflujo gastroesofágico crónico: El reflujo gastroesofágico crónico es un factor de riesgo importante para el desarrollo del esófago de Barrett y, por lo tanto, para el cáncer de esófago.
- Obesidad: La obesidad se ha asociado con un mayor riesgo de desarrollar cáncer de esófago.
- Consumo de tabaco: El consumo de tabaco es un factor de riesgo conocido para el cáncer de esófago.
La displasia de alto grado en el esófago de Barrett se considera una lesión precancerosa y se asocia con un mayor riesgo de desarrollar adenocarcinoma de esófago. El manejo de la displasia de alto grado depende de varios factores, incluyendo el tamaño y la ubicación de la lesión, así como la presencia de otras comorbilidades. Las opciones de tratamiento incluyen:
- Ablación endoscópica: La ablación endoscópica es un procedimiento que utiliza energía térmica o química para destruir la capa superficial del tejido que contiene la displasia de alto grado. La ablación endoscópica se puede realizar con técnicas como la terapia con láser, la terapia con plasma de argón, la terapia fotodinámica y la ablación con radiofrecuencia.
- Resección endoscópica: La resección endoscópica implica la eliminación de la lesión de displasia de alto grado a través de la endoscopia. Esta técnica puede ser útil para lesiones más grandes o para lesiones que no pueden ser tratadas con ablación endoscópica.
- Vigilancia endoscópica: Si la lesión es pequeña y no se considera apropiada para la ablación endoscópica o la resección endoscópica, la vigilancia endoscópica puede ser una opción. La vigilancia endoscópica implica la realización de biopsias de seguimiento en intervalos regulares para detectar cualquier cambio en la histología y descartar la progresión a cáncer de esófago.
- Cirugía: En casos seleccionados, la cirugía puede ser considerada para la displasia de alto grado. La cirugía implica la eliminación del esófago afectado y la reconstrucción del tracto gastrointestinal superior.
LINKS RECOMENDADOS:
EOA 2020 Lecture 5 Imaging in Barrett´s esophagus Sharma
Preguntas y respuestas:
Se debe tomar biopsia en pacientes con esofagitis Grado C o D y sospecha de Esofago de Barrett? Siempre que exista sospecha de esofago de Barrett se debe tomar biopsia independientemente del grado de esofagitis Cual es el biomarcador más utilizado en el esofago de Barrett? Es la displasia pero tiene limitaciones como que se puede presentar en parches, en algunas oportunidades no produce alteraciones visibles en la mucosa, la inflamación complica la interpretación de los hallazgos histopatológicos.



























































Article Comments