Clostridium difficile
- Es una bacteria anaerobia, gram negativa, formadora de esporas
- Coloniza el intestino en el 70% de neonatos y niños
- Puede formar parte de la flora comensal en el adulto
- No es patógeno en su ambiente natural
- Es la causa más común de diarrea asociada a medicamentos
- La diarrea puede ocurrir durante la administración del antibiótico o hasta 8 semanas posterior a suspender el medicamento

La edad mayor a 65 años es el factor de riesgo mas importante para el inicio de la infección, recurrencia y complicaciones

TIPS
Patogénesis
- El huésped susceptible se expone a las esporas producidas por el Clostridium difficile
- Luego se produce el sobrecrecimiento del Clostridium producto de la alteración de la flora normal intestinal por el uso de antibióticos de amplio espectro
- La colonización temporal puede llevar a la presencia de un estado de portador sano
- El efecto de las toxinas se traduce en la presencia de diarrea
Clasificación de acuerdo a severidad:

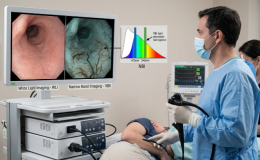
Hallazgos Endoscópicos:
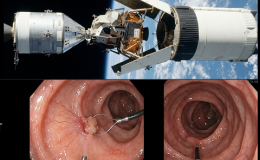
La colitis pseudomembranosa es una inflamación del colon causada por la infección de la bacteria Clostridium difficile. Los hallazgos endoscópicos característicos de la colitis pseudomembranosa incluyen los siguientes:
- Pseudomembranas: Las pseudomembranas son placas o membranas amarillentas o blanquecinas que se adhieren a la mucosa del colon. Estas pseudomembranas consisten en una mezcla de fibrina, células inflamatorias, moco y restos celulares. Pueden variar en tamaño y forma, y su apariencia puede asemejarse a la de costras o placas adheridas a la superficie de la mucosa.
- Eritema y edema: La mucosa colónica puede presentar enrojecimiento (eritema) y un aspecto hinchado o inflamado (edema). Estos cambios son indicativos de la inflamación que ocurre en la colitis pseudomembranosa.
- Fragilidad de la mucosa: La mucosa colónica puede volverse frágil y fácilmente desprendible debido a la inflamación. Esto puede llevar a la formación de pequeñas áreas de erosiones o úlceras en la superficie de la mucosa.
- Engrosamiento de la mucosa: En casos más severos de colitis pseudomembranosa, puede observarse un engrosamiento difuso de la mucosa colónica durante la endoscopia.
Es importante tener en cuenta que estos hallazgos endoscópicos pueden sugerir la presencia de colitis pseudomembranosa, pero el diagnóstico definitivo se realiza mediante pruebas de laboratorio para detectar la toxina producida por Clostridium difficile o mediante la visualización directa de las pseudomembranas en muestras de biopsias tomadas durante la endoscopia

La colitis pseudomembranosa consiste en placas amarillentas elevadas sobre mucosa inflamada. La mucosa alrededor de las placas es generalmente normal. En los casos severos la inflamación puede ser confluente. Generalmente no se producen úlceras
Tiene predilección por el recto y el colon sigmoides. Sin embargo algunos casos se pueden producir en el colon más proximal
Tratamiento:
- El metronidazol se utiliza como tratamiento de primera línea en casos de leve a moderada severidad. Sin embargo su eficacia en casos severos es cuestionable
- La Vancomicina se recomienda para casos severos y es más efectiva que el metronidazol. Se utiliza en forma endovenosa en combinación con metronidazol en casos severos
Transplante de materia fecal:
El trasplante de microbiota fecal (TMF) consiste en transferir heces de un donante sano a un individuo en que se piensa que existe una alteración de la microbiota colónica que produce enfermedad. El objetivo es restituir la Eubiosis es decir la microbiota saludable.
Se conoce con otros nombres:
- Trasplante de heces
- Trasplante fecal
- Reconstitución de la flora fecal
- Bacterioterapia fecal
- Infusión humana de probióticos
Mecanismo de Acción es desconocido pero puede estar relacionado a:
- Restitución de la función de la microbiota intestinal
- Estimulación de la respuesta inmune
Rutas de administración:
- Sonda nasogástrica
- Gastrostomía
- Sonda nasoduodenal/nasoyeyunal
- Endoscopia digestiva superior
- Colonoscopia (depositar heces en el colon derecho o el íleon terminal)
- Enema de retención
- Cápsulas
Criterios de Exclusión para donantes de microbiota fecal
Historia:
- Infección activa
- Exposición a antibióticos en los tres meses anteriores
- Viaje reciente con exposición a diarrea epidémica
- Historia de enfermedades gastrointestinales (enfermedad inflamatoria intestinal, síndrome de intestino irritable, diarrea crónica o estreñimiento, neoplasia gastrointestinal
- Historia de alergia o enfermedades autoinmunes
- Otros: factores de riesgo para enfermedad de Creutzfeldt-Jakob, diabetes, síndrome metabólico, síndromes de dolor crónica, exposición a medicamentos que puedan alterar la microbiota intestinal
- Consideraciones sociales: conductas de alto riesgo sexual, uso de drogas, residencia en sanatorios o cárceles, tatuaje o piercing en los últimos 6 meses
Análisis de las Heces:
Bacterias:
- Clostridium difficile
- Campilobacter
- Helicobacter pylori ( si el trasplante de microbiota se administra por vía oral)
- Salmonella
- Escherichia coli productora de la toxina shiga
- Shigela
- Otras consideraciones: Aeromonas, listeria monocytogenes, Yersinia, Vibrio cholerae y Vibrio parahaemolyticus
Virus:
- Rotavirus
- Norovirus
Parásitos:
- Criptosporidium
- Ciclospora
- Giardia
- Isospora
Pruebas sanguineas:
Bacterias:
- Sífilis
Virus:
- Hepatitis A,B,C
- HIV
Proceso de Recolección de la muestra
- El donante puede ser una persona relacionada o no relacionada con el receptor. Algunas investigaciones sugieren que el uso de donantes no relacionados se asocia a un microbioma diferente y que pudiese ser más efectivo para el reseteo de la microbiota del receptor.
- Se mezclan las heces con un líquido bacteriostático, se filtra y se administra al receptor.
- Se debe suspender la Vancomicina al menos 1 o 2 días previos al procedimiento.
- Se utilizan jeringas de 60 ml (4 o 5) administrando al menos 50 gramos de heces.
- Posterior al procedimiento se recomienda administrar loperamida sin embargo existe controversia a este respecto.
- Se puede colocar al paciente en posición de de Trendelenburg inversa durante una hora para aumentar la retención del material trasplantado.
Indicaciones para trasplante de Heces
- Infección recurrente por Clostridium difficile: Entre el 10 y 20% de pacientes desarrollan recurrencia en las primeras 8 semanas de tratamiento y 40 a 65% desarrollan múltiples recurrencias. Se han obtenido tasas de curación hasta del 90% según algunos trabajos.
- Enfermedad Inflamatoria Intestinal: los estudios han demostrado que existe disbiosis y disminución de la diversidad bacteriana en pacientes con esta patología.
- Otras indicaciones: síndrome de intestino irritable, síndrome de fatiga crónica, enfermedad de Parkinson, Obesidad, Síndrome metabólico y esclerosis múltiple.
Efectos adversos del trasplante de Heces
Menores: náuseas,vómitos (vía oral), dolor abdominal,gases,flatulencia,diarrea o constipación, febrícula.
Severos: relacionados con la sedación, infección, síndrome de intestino irritable postinfeccioso

Los efectos adversos son mas frecuentes cuando se administra por vía oral
Helicobacter pylori
Microbiológicamente, H. pylori corresponde a una bacteria espiroidea flagelada poseedora de la enzima ureasa, que le permite transformar urea a dióxido de carbono y amoníaco, con lo que alcaliniza el medio ácido en que se encuentra, atravesando la capa de mucus para finalmente alcanzar la superficie apical del epitelio gástrico

TIPS
- La infección del Helicobacter pylori es crónica y se adquiere durante la infancia

El Helicobacter pylori juega un papel importante en la patogenia del linfoma gástrico tipo MALT
La erradicación de la bacteria produce regresión del tumor en el 60-90% de los casos

TIPS
- Recomendación: la infección por Helicobacter pylori siempre causa gastritis, independientemente de los síntomas y complicaciones ( Agreement 100%,Grado A1) Maastricht VI 2022
Fenotipos:

La historia natural del Helicobacter puede llevar a gastritis, úlcera duodenal y cáncer
Recomendación: la infección por Helicobacter pylori siempre causa gastritis, independientemente de los síntomas y complicaciones ( Agreement 100%,Grado A1)Maastricht VI 2022
Helicobacter y cáncer gástrico:
- El adenocarcinoma tipo intestinal es el tipo más frecuente de cáncer gástrico y se desarrolla de la progresión de la gastritis cronica atrofica a metaplasia intestinal y displasia, como etapas previas a la transformación maligna.
- La metaplasia se define como la intestinizacion del epitelio gástrico normal en respuesta al daño crónico debido a infección por Helicobacter pylori o gastritis crónica autoinmune.

TIPS
- La atrofia gástrica se define como la pérdida de las glándulas nativas y tiene 2 causas principales: Infección por Helicobacter pylori y autoinmunidad
Patogenia:

El Helicobacter pylori produce daño inicialmente en la mucosa antral donde puede interactuar tanto en la superficie como a nivel de las células foveolares
Diagnóstico:

TIPS
- Recomendacion: el uso de aspirina o analgesicos antiinflamatorios no esteroideos (AINES) aumenta el riesgo de úlcera péptica y sus complicaciones en pacientes con Helicobacter pylori (Agreement 100%, Grado A1)
Pruebas invasivas:
Endoscopia Superior:
Existen hallazgos endoscópicos sugestivos de infección por Helicobacter pylori:
- Nodularidad: la nodularidad antral es un hallazgo frecuente en la infección por Helicobacter
- Pliegues gástricos engrosados
- Eritema: puede ser difuso o localizado
- Patrones vasculares: patrón de mosaico o en piel de serpiente
- Exudados o edemas
- Erosiones
- Cambios atróficos
- Xantomas
- La endoscopia superior se utiliza frecuentemente para el diagnóstico de infección por Helicobacter pylori
- La biopsia gástrica se considera la prueba de oro para el diagnóstico de esta patología
- Algunos sugieren tomar 5 biopsias para aumentar la sensibilidad del estudio: curvatura mayor y menor de cuerpo gástrico, incisura, curvatura mayor y menor del antro. Se deben colocar en 2 frascos separados
- Obtener biopsias de cuerpo es de particular importancia en pacientes que reciben tratamiento con inhibidores de bomba de protones por la migración proximal de la bacteria en estos casos
- Se puede utilizar hematoxilina eosina, Giemsa, Warthine-Starry
Pruebas no invasivas:
- Se incluye las pruebas serológicas de anticuerpos, antígeno en heces y prueba del aliento
- La prueba del aliento se basa en la capacidad de ureasa para convertir la solución de urea ingerida por el paciente en dióxido de carbono y urea. Es más sensible en pacientes sin antecedentes de gastrectomía o ingesta reciente de inhibidores de bomba de protones y antibióticos
- La prueba en heces tiene alta sensibilidad y especificidad, se puede aplicar tanto en niños como en adultos. Para los niños es más efectivo utilizar anticuerpos monoclonales que policlonales. Hay 2 tipos de prueba en heces, uno basado en pruebas enzimáticas y el otro por inmunocromatografía que tiene mayor sensibilidad diagnóstica. Puede afectarse en caso de uso de antibióticos y hemorragia digestiva
- La prueba en suero detecta anticuerpos en suero, saliva y orina. Es una prueba económica y detecta anticuerpos IgG que pueden estar presentes unas semanas después de adquirir la infección pero no es tan efectivo en el caso de infección activa

La determinación de Pepsinógeno I y la relación Pepsinógeno I/Pepsinógeno II en la deteccion de cancer gastrico (Sensibilidad: 56-69%, Especificidad: 71-73%) tiene baja sensibilidad en la detección de gastritis atrófica y metaplasia intestinal en poblaciones de alto riesgo por lo que no se recomienda actualmente
Para la prueba del aliento se recomienda suspender los inhibidores de bomba de protones 2 semanas previas al examen y los antibióticos 4 semanas antes del examen
La prueba en heces solo detecta infección aguda por Helicobacter

TIPS
- Recomendación: en pacientes jóvenes con dispepsia (Edad menor a 50 años) sin factores de riesgo específicos y sin signos de alarma se recomienda pruebas no invasivas para el diagnóstico de la infección por Helicobacter pylori ( Agreement 97%,Grado A1)Maastricht VI 2022
- Recomendación: Realizar prueba no invasiva y tratar es una estrategia apropiada para el paciente con dispepsia no investigada ( Agreement 94%,Grado A1) Maastricht VI 2022
Tratamiento:
El tratamiento ha ido evolucionando de acuerdo al aumento de la resistencia bacteriana
Terapias tradicionales:
- Terapia cuádruple con Bismuto: representa la piedra angular del tratamiento para el Helicobacter pylori especialmente en regiones con alta resistencia antibiótica. Incluye un inhibidor de bomba de protones, bismuto, metronidazol y tetraciclina
- Terapia triple con Claritromicina: incluye inhibidor de bomba de protones, claritromicina, amoxicilina o metronidazol. Se recomienda en regiones donde la resistencia a Claritromicina es menor al 15% y en pacientes sin exposición previa a Macrólidos
- Cápsula 3-1: contiene Bismuto, Metronidazol y tetraciclina en una sola cápsula la que ha demostrado alta efectividad en áreas con alta resistencia a Claritromicina o Metronidazol
- Terapias basadas en Vonoprazan: el Vonoprazan, que en un bloqueador selectivo de los canales de potasio, se ha incorporado a la terapia triple (Vonoprazan, Amoxicilina y Claritromicina o Metronidazol) con buena efectividad en regiones con alta resistencia antibiótica
Terapias emergentes y terapia no antibiótica:
- Probióticos: se utilizan en combinación con antibióticos para mejorar la erradicación y reducir los efectos adversos. Modulan la microbiota intestinal y mejoran la tolerabilidad
- Vacunas: la investigación en cuanto a la producción de vacunas se encuentra en investigación con el objeto de prevenir la infección y reducir la necesidad de tratamientos de erradicación
- Nanotecnología: mejora en los sistemas de administración de medicamentos mediante el uso de nanomateriales dirigidos directamente a la bacteria lo que permite reducir la resistencia antibiótica
Tratamiento personalizado:
- Pruebas de susceptibilidad
Tratamiento alternativo:
- Modificación del microambiente gástrico: alterar el contenido de Oxigeno a nivel Gástrico puede disminuir la sobrevida de la bacteria
Tratamiento de primera línea:
- La terapia cuádruple con Bismuto representa la opción de primera línea en especial en regiones resistencia elevada a Claritromicina
- La terapia con Vonoprazan (doble o triple) es altamente efectiva y se puede comparar a la terapia cuádruple con bismuto. Se prefiere la terapia doble porque tiene menos efectos colaterales y menor dosis de antibióticos

La dosis óptima de subcitrato de Bismuto es de 240 mgs cada 8 horas (esquema cuádruple) con lo que se obtiene tasas elevadas de erradicación. La dosis de subsalicilato es de 600 mgs cada 8 horas, sin embargo su papel en la erradicación es menos definida y estudiada
La infección por Helicobacter se adquiere en épocas tempranas de la vida, la bacteria tiene el estómago como hábitat natural, por lo tanto se ha expuesto a una gran cantidad de antibióticos que se consumen vía oral

TIPS
- El bismuto tiene efecto bactericida porque forma complejos en la pared celular que inhibe varias enzimas, la síntesis de ATP y la adherencia bacteriana a la mucosa gástrica. Altera los sistemas de defensa por inhibición de la catalasa y la superóxido dismutasa. Impide la entrada de protones a la bacteria lo que mantiene un pH neutro lo que mejora la efectividad antibiótica. Produce alteraciones en el metabolismo del hierro que es fundamental en el metabolismo bacteriano
- Los efecto adversos del bismuto son al neurotoxicidad a dosis elevadas y que mejoran al suspender el medicamento. Puede producir náuseas, vómitos, diarrea, dolor abdominal, dolor de cabeza y mareos
- El Vonoprazan es un bloqueador competitivo del potasio, actúa inhibiendo el sistema de ATPasa a nivel de las células parietales lo que bloquea la producción de ácido. A diferencia de los inhibidores de bomba de protones no requiere activación por el ácido y se une de manera no covalente y reversible a las bombas de protones. Tienen rápido comienzo de acción con supresión de ácido entre 2-3 horas de su administración con efecto sostenido durante 24 horas. Representa una excelente opción en tratamiento de primera y segunda línea para erradicación de Helicobacter
Tratamiento de segunda línea:
Qué relación existe entre la presencia de xantomas gástricos e infección por Helicobacter? Los xantomas gástricos se asocian a inflamación crónica e infección por Helicobacter. Son lesiones frecuentes a mayor edad, predominan en el género masculino y se asocian a la atrofia gástrica y metaplasia intestinal. Pueden asociarse a dislipidemia Cuales son las ventajas de la prueba del aliento para el diagnostico de infección por Helicobacter pylori? Es una prueba no invasiva, tiene alta sensibilidad y especificidad tanto antes como después del tratamiento, es segura ya que utiliza el Carbono 13 que es un isótopo estable que puede ser utilizado incluso en niños y mujeres embarazadas, es efectivo para confirmar la erradicación de la bacteria y es fácil de utilizar Cuales son las desventajas de la prueba del aliento para el diagnóstico de infección por Helicobacter pylori? Es una prueba costosa que requiere equipo de espectrometría para su análisis, tiene falsos negativos (uso de inhibidores de bomba previos, se recomienda suspenderlos 14 días antes. El uso de antibióticos también puede alterar la prueba), no da información acerca de la densidad de la bacteria lo que no establece la severidad de la infección, existe variabilidad en cuanto a los protocolos utilizados y ciertas condiciones médicas que pueden alterar los resultados (pacientes gastrectomizados y pacientes con hemorragia digestiva)


























Article Comments