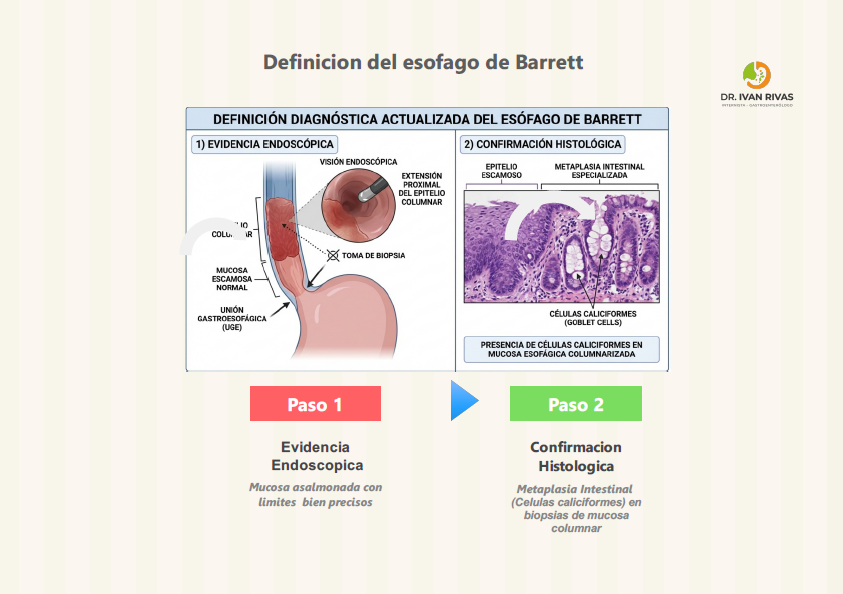
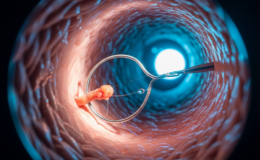
- Es una condición en la que el epitelio escamoso del esofago distal es substituido por epitelio columnar tipo intestinal (metaplasia intestinal especializada). Es el reemplazo del epitelio normal del esófago por células que tienen similitud con el epitelio del intestino delgado
- 1 al 2% de la población de los Estados Unidos tienen EB
- Está relacionado con el aumento de la incidencia de obesidad en Estados Unidos
- El EB ocurre en pacientes con o sin síntomas de enfermedad de reflujo. Cerca de la mitad de los pacientes con EB no tienen síntomas de reflujo
- La mayor parte de las veces el EB no se detecta
- Se relaciona con la exposición del esófago a reflujo ácido o biliar
La progresión de metaplasia, displasia de bajo grado, displasia de alto grado y adenocarcinoma no se cumple de manera secuencial en muchos pacientes. Existe un riesgo aproximado para desarrollar cáncer entre 0.3-0.5% al año
Estudios recientes han demostrado que en la minoría de pacientes el cáncer se desarrolla siguiendo la secuencia tradicional en la cual existen alteraciones genéticas o epigenéticas que inactivan los genes supresores y activan los oncogenes lo cual produce inestabilidad genómica. Pareciera que la mayoría de los pacientes con cáncer presentan una mutación del gen p53. Quiere decir que existen pacientes con cáncer en los que no se tienen antecedentes de displasia
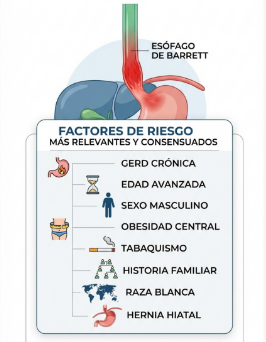
Factores de Riesgo para Esofago de Barrett
La American Gastroenterological Association (AGA) recomienda considerar el cribado con endoscopia digestiva alta en individuos que presenten al menos 3 factores de riesgo establecidos para esófago de Barrett y adenocarcinoma esofágico. Los factores de riesgo reconocidos incluyen:
- Sexo masculino
- Raza blanca no hispana
- Edad >50 años
- Antecedente de tabaquismo
- Enfermedad por reflujo gastroesofágico (ERGE) crónica (>5 años o síntomas semanales o más frecuentes)
- Obesidad
- Antecedente familiar de esófago de Barrett o adenocarcinoma esofágico
Cabe destacar que la AGA ha reducido la importancia de la ERGE como requisito obligatorio para el cribado, ya que hasta el 54.9% de los pacientes con adenocarcinoma esofágico en EE.UU. no habrían sido identificados por las guías previas que exigían ERGE sintomática como criterio indispensable. La prevalencia de esófago de Barrett en la población con ERGE es de aproximadamente 3%, pero aumenta con cada factor de riesgo adicional. La prevalencia más alta se observó en pacientes con antecedente familiar de Barrett/adenocarcinoma esofágico junto con ERGE (23.4%).
Efecto acumulativo de los factores de riesgo:
Según la guía del American College of Gastroenterology (ACG), existe una relación lineal positiva entre el número de factores de riesgo y la prevalencia de esófago de Barrett: cada factor de riesgo adicional incrementa la prevalencia en un 1.2%. La prevalencia en pacientes con ERGE sola es del 2.3%, pero asciende al 12.2% cuando se asocia al menos un factor de riesgo adicional.
Obesidad y adiposidad central:
La guía de la American Society for Gastrointestinal Endoscopy (ASGE) señala que, si bien la obesidad general (medida por IMC) no mostró una asociación significativa en un metaanálisis de 11 estudios, la adiposidad central sí se asoció de forma significativa con el esófago de Barrett. La obesidad actúa como factor de riesgo tanto por mecanismos mecánicos (aumento de la presión intragástrica) como por mecanismos inflamatorios mediados por citoquinas del tejido adiposo visceral.
Predominio masculino y progresión:
Existe un marcado predominio masculino tanto en el esófago de Barrett (67% hombres vs. 33% mujeres) como en el adenocarcinoma esofágico (89% vs. 11%). El riesgo de progresión a adenocarcinoma es significativamente mayor en hombres (OR ajustado 2.2; IC 95%: 1.8–2.5).
Diagnostico del Esofago de Barrett
La American Gastroenterological Association (AGA) recomienda que el diagnóstico de esófago de Barrett se base en dos componentes fundamentales: hallazgos endoscópicos y confirmación histológica.
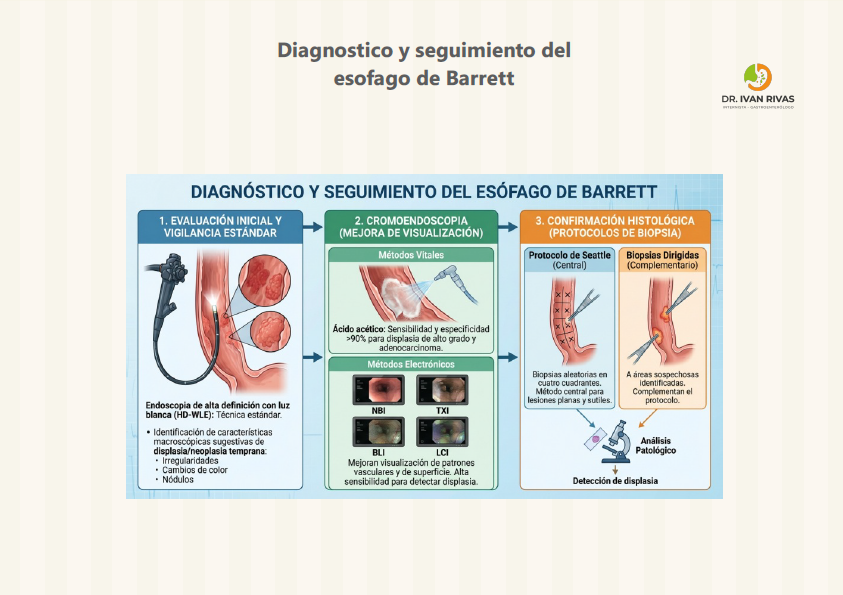
Evaluación endoscópica:
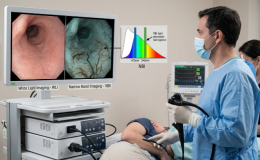
Los exámenes de cribado y vigilancia deben realizarse con endoscopia de alta definición con luz blanca (HD-WLE) y cromoendoscopia virtual (como NBI, Narrow-Band Imaging), dedicando tiempo adecuado a la inspección del segmento de Barrett. La extensión del esófago de Barrett debe documentarse utilizando la clasificación de Praga (C M), que registra la extensión circunferencial (C) y la extensión máxima (M) de la mucosa columnar por encima de la unión gastroesofágica, junto con una descripción clara de los puntos de referencia anatómicos y las lesiones visibles (nodularidad, ulceración, placas, áreas de depresión).
Protocolo de biopsias (Protocolo de Seattle):
La toma de muestras debe realizarse siguiendo el protocolo de Seattle: biopsias en los 4 cuadrantes cada 1–2 cm a lo largo del segmento de Barrett, desde la unión escamocolumnar hasta el esfínter esofágico inferior, además de biopsias dirigidas de cualquier lesión visible. Este protocolo estructurado se asocia con una tasa de detección de displasia 2.75 veces mayor en comparación con biopsias no sistemáticas. Sin embargo, las tasas de adherencia al protocolo de Seattle son subóptimas (aproximadamente 49%), y la probabilidad de no adherencia aumenta un 31% por cada centímetro adicional de longitud del Barrett.
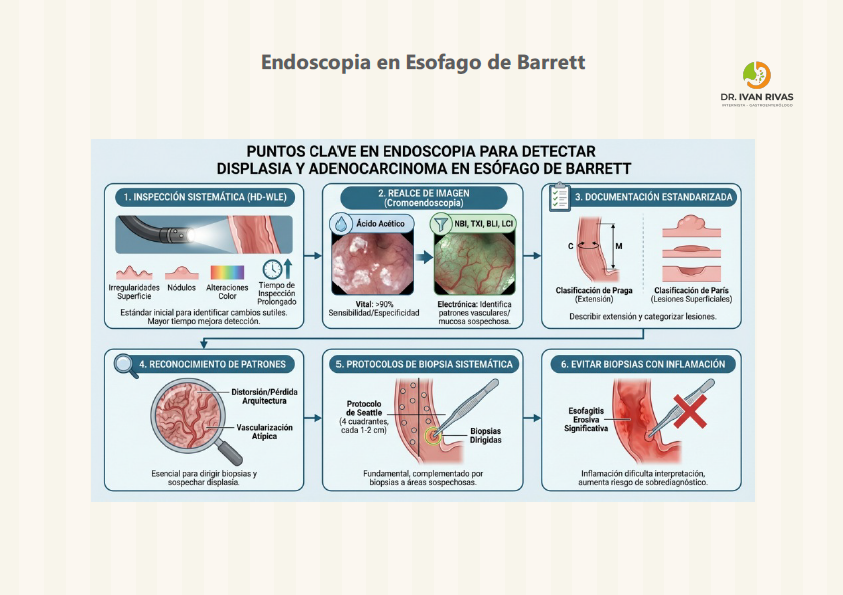
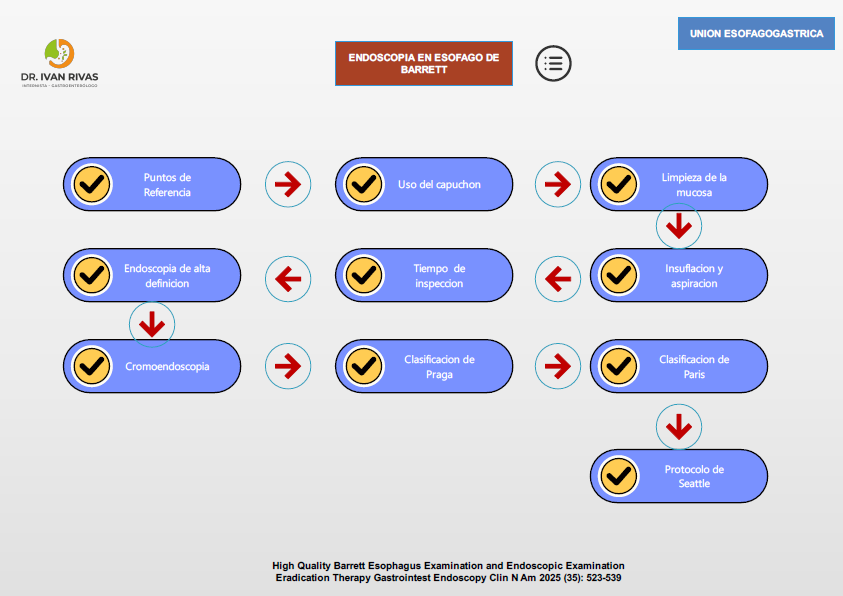
Endoscopia en Esofago de Barrett
La endoscopia superior es la herramienta más eficaz para el diagnóstico de esófago de Barrett.
Para el diagnóstico de esófago de Barrett se requiere endoscopia y biopsia: el endoscopista debe documentar que el epitelio columnar se extiende por encima de la unión gastroesofágica del esófago distal y la biopsia debe demostrar metaplasia intestinal.
Para diagnosticar el esófago de Barrett la unión escamocolumnar y la unión gastroesofágica deben ser identificadas.
El esofago de Barrett se puede clasificar como esofago de Barrett corto cuando la distancia entre la línea Z y la unión gastroesofágica es menor a tres centímetros o esófago de Barrett largo cuando la distancia es mayor a 3 centímetros
Criterios diagnosticos para el esofago de Barrett
La guía actualizada del American College of Gastroenterology (ACG) de 2022 establece que el diagnóstico de esófago de Barrett requiere: (1) mucosa columnar de al menos 1 cm de longitud en el esófago tubular, y (2) metaplasia intestinal con células caliciformes en las biopsias.
Los pacientes con una línea Z de aspecto normal o con desplazamiento proximal <1 cm desde la parte superior de los pliegues gástricos no deben someterse a biopsias de rutina, ya que los criterios de Praga no son fiables para segmentos <1 cm y el riesgo de progresión es muy bajo.
Consideraciones previas a la endoscopia:
- En caso de Esofagitis por Reflujo Grado B-D (Clasificación de los Angeles) se recomienda tratamiento médico por 8-12 semanas con inhibidores de bomba de protones y endoscopia superior control al finalizar tratamiento
Puntos de Referencia:
- Hiato diafragmatico: estrechamiento donde el esofago atravieza el diafragma
- Union esofagogastrica: extensión proximal de los pliegues gástricos
- Unión escamocolumnar o línea Z: transición entre el epitelio blanquecino del esofago y el rosado del estómago
Uso del Capuchón o Cap:
Limpieza:
- Si no se limpia bien es imposible la detección de lesiones más pequeñas en el EB
- La mucosa debe estar libre de moco, saliva, detritos para permitir la exploración cuidadosa del patrón vascular y mucoso
- Se puede utilizar waterjet para limpiar el segmento de Barrett (1-2 minutos), para determinar si se ha logrado una buena limpieza se pasa a cromoscopia óptica y NBI
Insuflación y aspiración:
Tiempo de inspección:
- El tiempo de inspección endoscópica es un factor crítico para el diagnóstico y la vigilancia del esófago de Barrett, ya que se asocia directamente con la capacidad de detectar lesiones preneoplásicas y neoplásicas, especialmente displasia de alto grado y adenocarcinoma esofágico en etapas tempranas. La evidencia demuestra que una inspección meticulosa y prolongada del segmento de Barrett incrementa significativamente la tasa de detección de lesiones sospechosas y de neoplasia avanzada. En particular, se ha observado que endoscopistas que dedican más de 1 minuto por centímetro de segmento de Barrett detectan un mayor porcentaje de pacientes con lesiones endoscópicamente sospechosas (54.2% vs 13.3%) y muestran una tendencia hacia una mayor detección de neoplasia avanzada (40.2% vs 6.7%) en comparación con quienes dedican menos tiempo
- La importancia de este hallazgo radica en que una proporción considerable de neoplasias asociadas a Barrett pueden ser pasadas por alto durante la endoscopía inicial si la inspección es insuficiente, lo que se traduce en diagnósticos tardíos y peores resultados clínicos. Por ello, las guías de práctica clínica recomiendan explícitamente dedicar un tiempo adecuado a la inspección del segmento de Barrett, sugiriendo como estándar un mínimo de 1 minuto por centímetro de mucosa circunferencial y una duración total de la endoscopía superior a 7 minutos para maximizar el rendimiento diagnóstico
- En conclusión, asegurar un tiempo de inspección suficiente durante la endoscopía es una medida sencilla y ampliamente disponible que mejora la calidad del examen y la detección de displasia y cáncer en el esófago de Barrett, constituyendo un indicador de calidad en la práctica endoscópica
Luz blanca, endoscopia de alta definición y cromoendoscopia:
- La luz blanca estándar ha sido la base de la endoscopia para el diagnóstico y vigilancia del esófago de Barrett, permitiendo la identificación de la mucosa columnar y lesiones evidentes como nódulos, ulceraciones o áreas de irregularidad. Sin embargo, su resolución limitada puede dificultar la detección de displasia o neoplasia sutiles, especialmente en etapas tempranas
- La endoscopia de alta definición (HD-WLE) representa una mejora significativa respecto a la luz blanca estándar, ya que proporciona imágenes con mayor resolución y detalle, lo que incrementa la capacidad de detectar lesiones preneoplásicas y neoplásicas. El uso de HD-WLE está asociado con una mayor tasa de detección de displasia y adenocarcinoma en comparación con sistemas de definición estándar, y se considera el estándar de atención en la vigilancia del esófago de Barrett. Además, la inspección meticulosa y prolongada con HD-WLE aumenta la sensibilidad para identificar lesiones sutiles
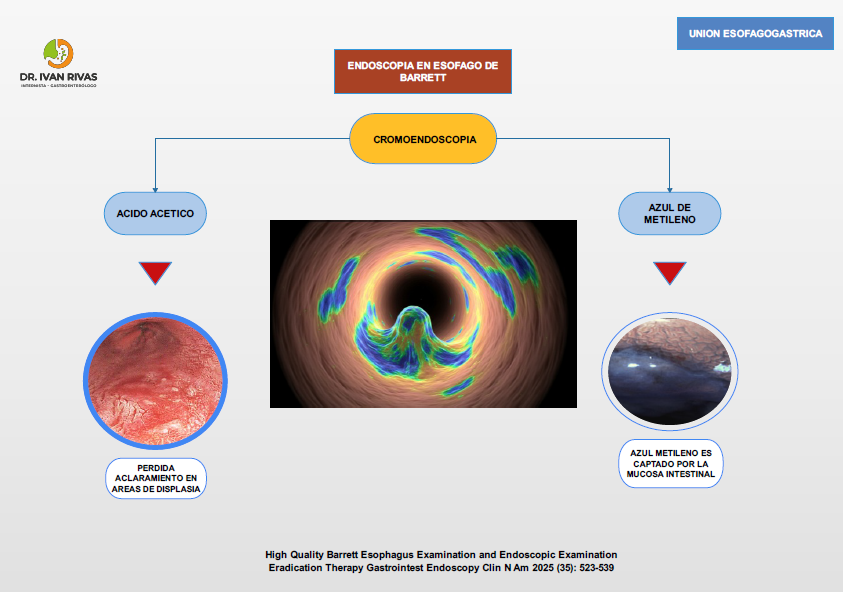
- La cromoendoscopia, tanto vital (ácido acético) como electrónica (virtual chromoendoscopy, por ejemplo NBI, i-Scan, LCI), aporta ventajas adicionales al realzar el contraste de la superficie mucosa y los patrones vasculares. Estas técnicas permiten una mejor visualización de áreas sospechosas, facilitando la identificación de displasia y adenocarcinoma temprano. La cromoendoscopia electrónica, disponible en la mayoría de los endoscopios modernos, incrementa la tasa de detección de displasia en un 10–20% respecto a HD-WLE sola, y mejora la caracterización de lesiones, lo que optimiza el rendimiento de las biopsias dirigidas
La imagen de banda estrecha (NBI) en el esófago de Barrett permite una caracterización detallada de los patrones mucosos y vasculares, facilitando la identificación de metaplasia intestinal y displasia de alto grado o adenocarcinoma. Los hallazgos característicos con NBI se basan en la evaluación de la regularidad de los patrones mucosos y vasculares:
Metaplasia intestinal (Barrett no displásico): Se observa un patrón mucoso regular, típicamente de tipo velloso, tubular o lineal, acompañado de un patrón vascular regular. Estos patrones se asocian con una alta probabilidad de metaplasia intestinal y baja probabilidad de displasia
Displasia de alto grado y adenocarcinoma: Los hallazgos clave son la presencia de patrones mucosos irregulares o distorsionados y patrones vasculares irregulares o anormales. Esto incluye la pérdida de la arquitectura normal, distorsión de las criptas, interrupción de la superficie, y vasos sanguíneos anormales, como vasos dilatados, tortuosos o de distribución irregular. La presencia de uno o más de estos hallazgos se correlaciona fuertemente con displasia de alto grado o cáncer
Clasificación simplificada: El sistema BING y otras clasificaciones validadas dividen los patrones en “regulares” (baja probabilidad de displasia) e “irregulares” (alta probabilidad de displasia o neoplasia), lo que permite una evaluación rápida y reproducible con alta sensibilidad y especificidad para la detección de displasia y adenocarcinoma
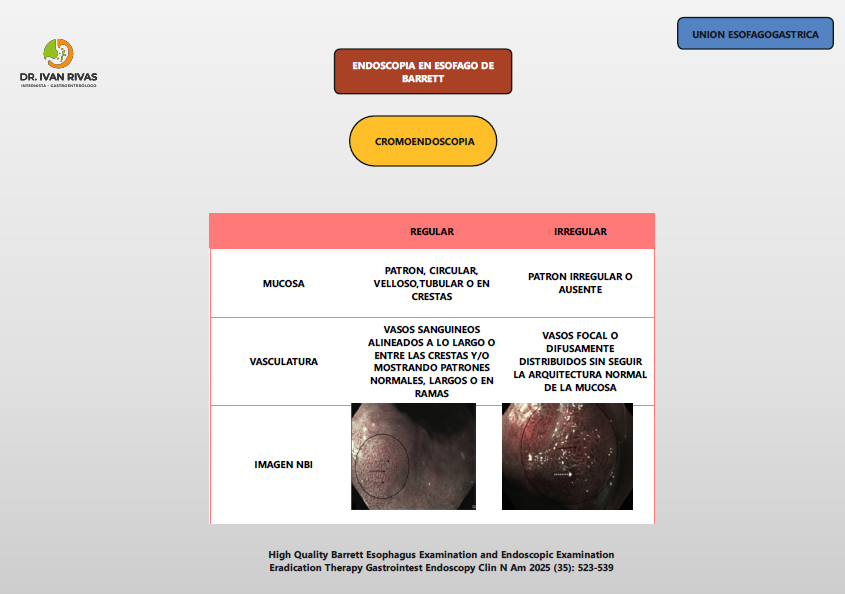
La clasificación BING (Barrett’s International NBI Group) para el esófago de Barrett es un sistema internacionalmente validado que utiliza la imagen de banda estrecha (NBI) para identificar y categorizar la presencia de displasia y adenocarcinoma esofágico en pacientes con esófago de Barrett. Esta clasificación se basa en la evaluación de los patrones mucosos y vasculares observados durante la endoscopía con NBI, y su objetivo es distinguir entre mucosa no displásica y mucosa con displasia o neoplasia
- Patrones regulares: Incluyen patrones mucosos y vasculares que mantienen una arquitectura uniforme y ordenada. Los patrones mucosos regulares pueden ser de tipo villoso, tubular o lineal, y los vasos sanguíneos presentan trayectorias rectas y distribución homogénea. Estos hallazgos se asocian con mucosa no displásica o metaplasia intestinal, y tienen una baja probabilidad de displasia.
- Patrones irregulares: Se caracterizan por una alteración significativa de la arquitectura mucosa y vascular. Los patrones mucosos muestran distorsión, pérdida de la estructura, interrupción de las criptas o áreas de erosión, mientras que los vasos sanguíneos presentan trayectorias tortuosas, dilatación, ramificación anormal o distribución caótica. Estos hallazgos se correlacionan con una alta probabilidad de displasia de alto grado o adenocarcinoma esofágico
La clasificación BING ha demostrado alta precisión diagnóstica, con sensibilidad y especificidad superiores al 80% para la detección de displasia y neoplasia, y un elevado nivel de concordancia interobservador
Criterios de Praga
- Los criterios de Praga (Prague C & M criteria) constituyen el sistema estandarizado internacionalmente para la clasificación endoscópica del esófago de Barrett. Este sistema documenta de manera precisa la extensión de la mucosa columnar en el esófago, permitiendo una comunicación clara entre endoscopistas y facilitando la vigilancia y el seguimiento longitudinal de la enfermedad
Los criterios de Praga se basan en dos mediciones principales:
- C (circunferencial): Longitud en centímetros de la extensión circunferencial continua de la mucosa columnar por encima de la unión gastroesofágica (GEJ).
- M (máxima): Longitud en centímetros de la extensión máxima (incluyendo lengüetas o islotes) de la mucosa columnar por encima de la GEJ.
Para aplicar correctamente los criterios, se deben identificar tres puntos anatómicos endoscópicos:
- El hiato diafragmático
- La unión gastroesofágica (GEJ), definida por el punto más proximal de los pliegues gástricos
- La unión escamocolumnar (línea Z)
La medición se realiza con mínima insuflación, documentando primero la extensión circunferencial (C) y luego la máxima (M), incluyendo cualquier lengüeta o islote proximal a la extensión circunferencial. Además, se recomienda registrar la presencia, tamaño y localización de islotes de mucosa columnar, así como la localización de lesiones visibles (nódulos, ulceraciones, áreas de depresión)
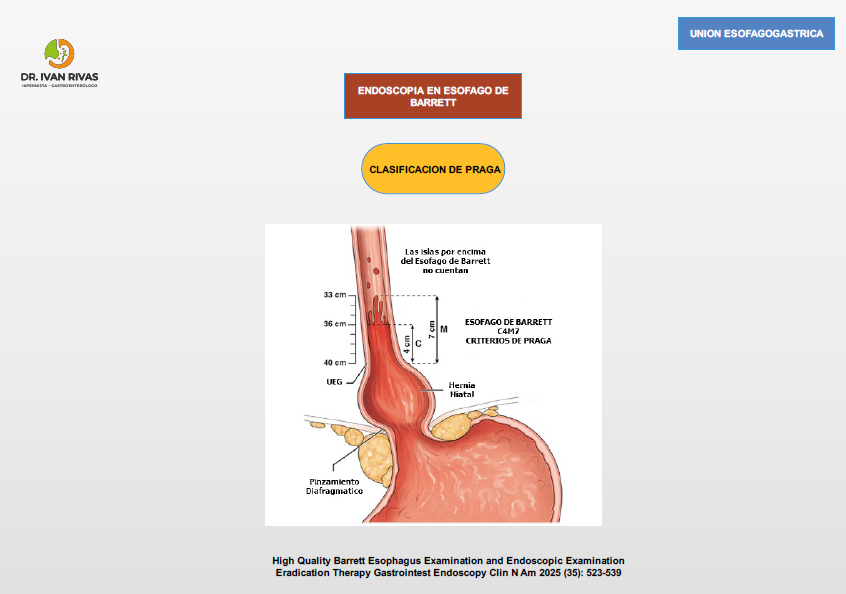
- La criterios de Praga se desarrolló para estandarizar la clasificación del esofago de Barrett. En esta clasificación la longitud máxima (M) (incluyendo las lenguetas) del esofago de Barrett y la longitud circunferencial del segmento de Barrett (C) se miden durante el procedimiento endoscópico. El resultado obtenido puede ser utilizado para el seguimiento del Esofago de Barrett.
- Es un procedimiento validado cuando el segmento de Barrett es mayor a 1 cm
- Lo primero es determinar la posición real de la union esofagogastrica que es a nivel del límite proximal de los pliegues gástricos (Origen: 0 cms). Luego determinar la extensión circunferencial de la metaplasia (C: 4 cms). Si existe prolongación proximal se determina la extensión máxima de la metaplasia (M: 7 cms)
La fiabilidad interobservador de los criterios de Praga es alta para segmentos ≥1 cm (coeficiente de fiabilidad >0.9), pero disminuye para segmentos <1 cm, por lo que la mayoría de las guías internacionales establecen un umbral de ≥1 cm para el diagnóstico endoscópico de esófago de Barrett
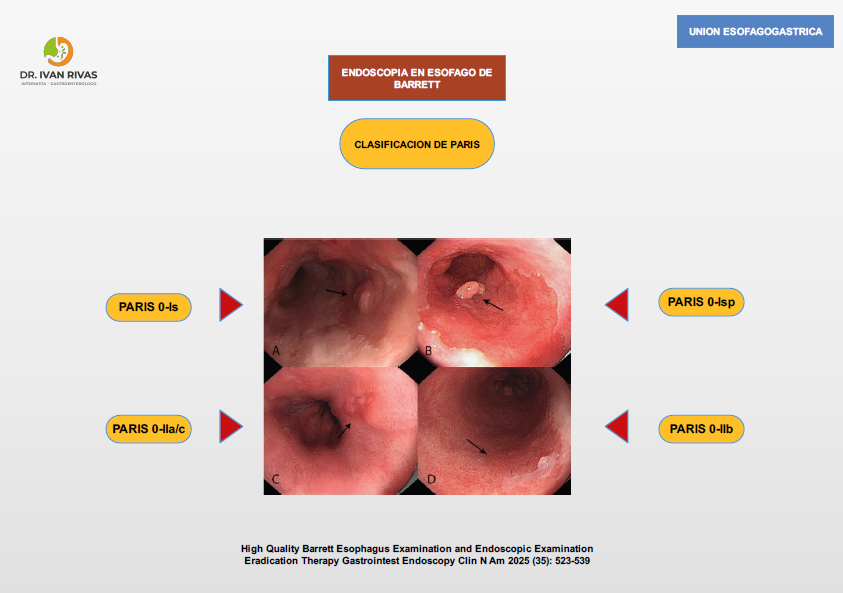
Clasificación de Paris
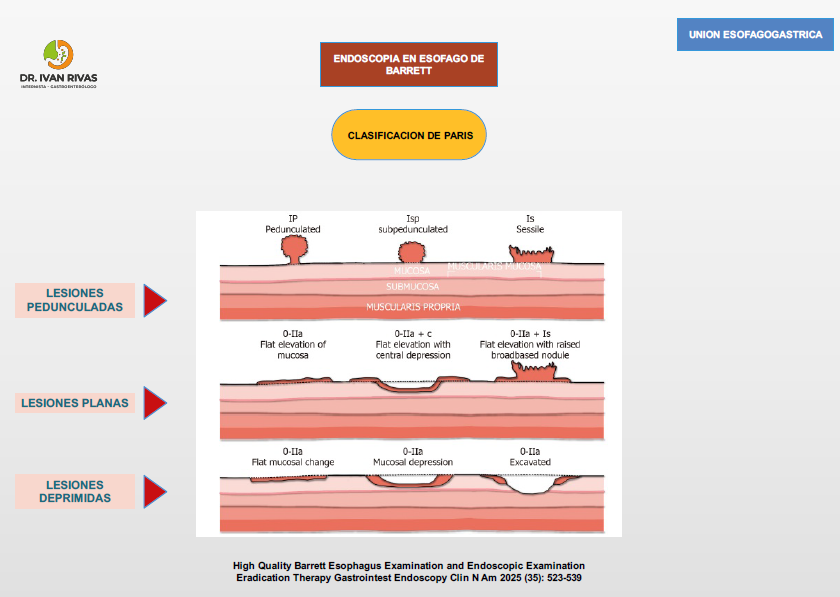
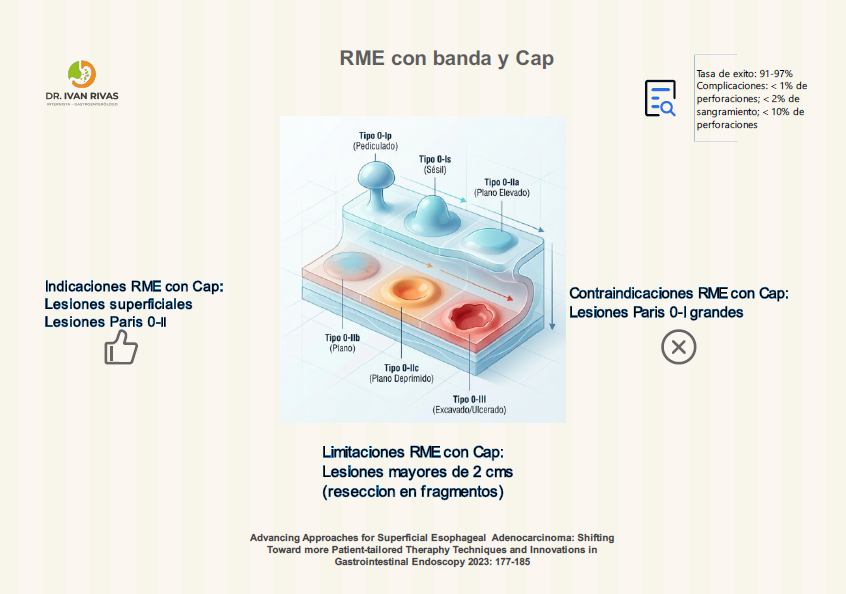
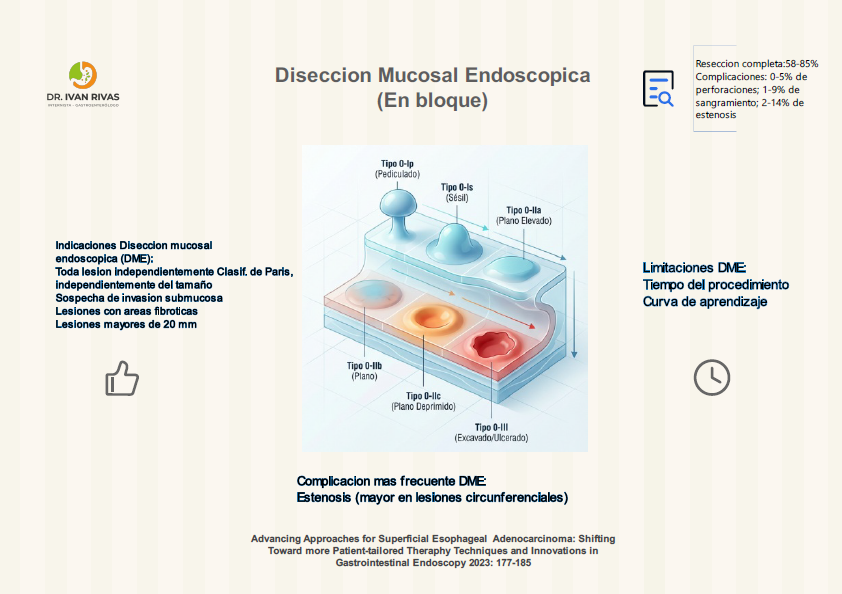
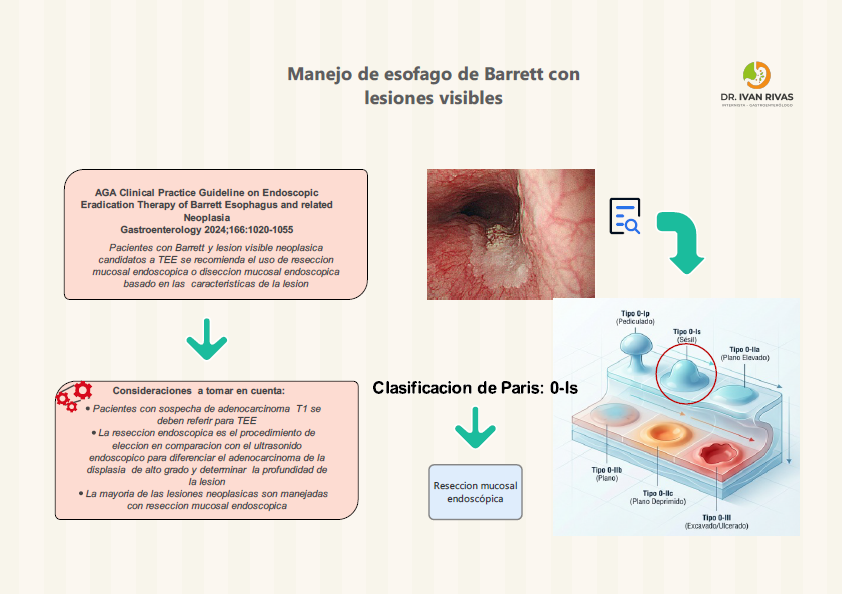
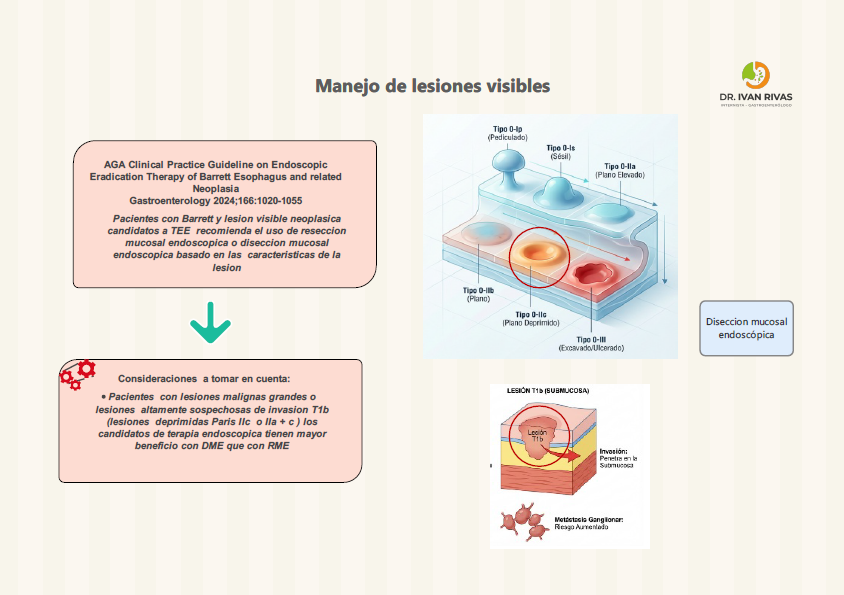
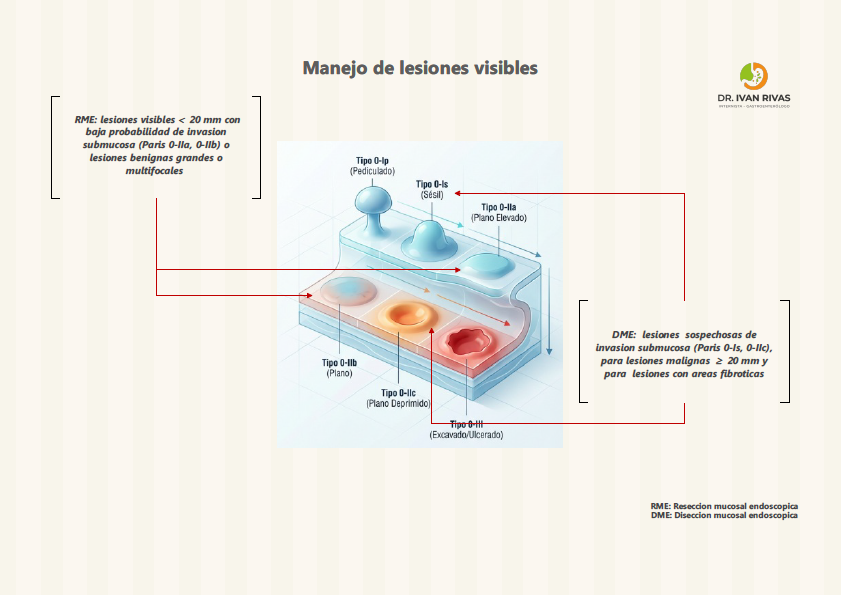
La Clasificación de París es el sistema estandarizado recomendado por la ACG, AGA, ESGE y la World Endoscopy Organization (WEO) para describir la morfología endoscópica de las lesiones neoplásicas superficiales (tipo 0) en el esófago de Barrett. Su importancia radica en que permite estimar la profundidad de invasión y orientar la decisión terapéutica (resección endoscópica vs. quirúrgica).
La clasificación de París tiene valor pronóstico para predecir la profundidad de invasión, aunque la ACG advierte que estas correlaciones no son perfectas y no deben sustituir la evaluación histopatológica del espécimen resecado.
Las lesiones Paris 0-I y 0-IIc tienen mayor probabilidad de invadir la submucosa.
La guía de la ASGE (2023) recomienda que todas las lesiones sospechosas de albergar cáncer, incluyendo las tipo 0-I y 0-IIa+c, deben ser resecadas en bloque cuando sea posible para una estadificación histológica precisa.
La AATS (2025) refuerza que las lesiones 0-II son generalmente mucosas, las 0-I pueden ser mucosas o submucosas, y las 0-III infiltran la capa muscular, por lo que no son aptas para resección endoscópica.
La ESGE recomienda que todos los endoscopistas que realizan endoscopia digestiva alta deben entrenarse en el uso de la clasificación de París para describir lesiones sospechosas de neoplasia tanto en epitelio de Barrett como en epitelio escamoso.
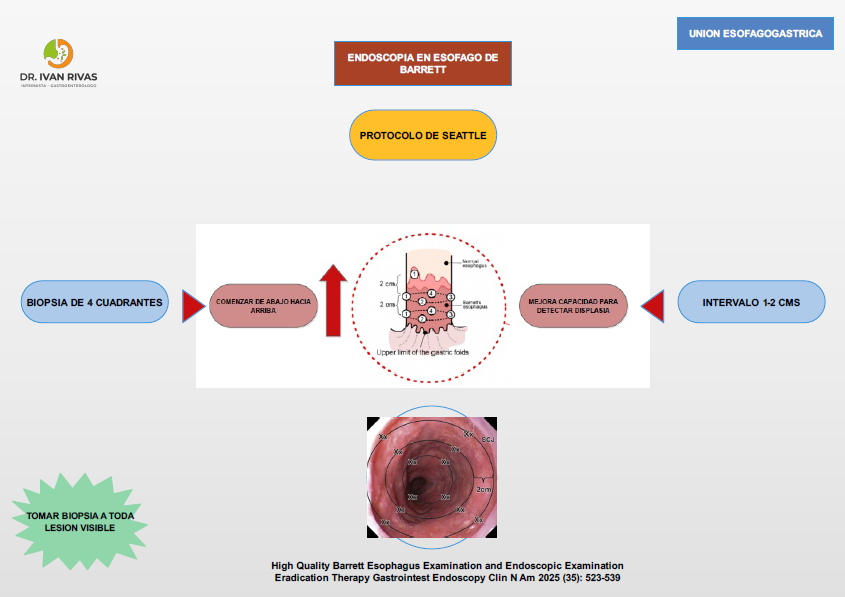
Protocolo de Seattle:
- En pacientes con sospecha de EB al menos 8 biopsias aleatorias deben ser obtenidas para maximizar la histología. En pacientes con segmento corto (1-2 centímetros) en la cual es difícil obtener las 8 muestras se deben tomar al menos 4 muestras circunferenciales y una biopsia por lengüeta de EB
- Las lesiones sospechosas deben ser biopsiadas y enviadas en frasco separado
- Si la biopsia demuestra metaplasia intestinal se confirma el diagnóstico de esófago de Barrett.
- Lo primero es observar con luz blanca, endoscopio de alta definición y cromoendoscopia. Buscar cualquier cambio de patrón, áreas de neovascularización, nódulos, depresiones, etc
- Hacer énfasis en la pared derecha y el segmento proximal (en especial en segmentos largos)
- Utilizar capuchón
- Hacer énfasis en la región más proximal porque allí puede existir displasia
- Se debe tomar biopsias en los 4 cuadrantes cada 1-2 centímetros
- La adherencia al protocolo de Seattle es baja
- A pesar de usar este protocolo entre el 94-96% de la mucosa no se analiza
El análisis histopatológico debe ser hecho por un patólogo con experiencia en Barrett
Toma de biopsias en pacientes con linea Z irregular:
La ACG y la AGA recomiendan no realizar biopsias de rutina de una línea Z normal o irregular en ausencia de anomalías mucosas visibles, por varias razones:
- Riesgo de progresión prácticamente nulo: En un estudio multicéntrico de 1,791 pacientes seguidos durante una mediana de 5.9 años, ninguno de los 167 pacientes con línea Z irregular (<1 cm) desarrolló displasia de alto grado (DAG) ni adenocarcinoma esofágico (ACE), en comparación con una tasa de progresión de 7.9/1,000 personas-año en pacientes con Barrett ≥1 cm. Un estudio poblacional de Olmsted County con 86 pacientes con MI de la UGE seguidos durante 8 años tampoco mostró progresión a DAG o ACE
- Baja reproducibilidad: El coeficiente de fiabilidad de los criterios de Praga para segmentos <1 cm es de solo 0.22 (concordancia pobre), incluso entre endoscopistas expertos, lo que hace que la medición sea poco confiable
Cuando biopsiar la línea Z?
- La única excepción es cuando se identifican anomalías mucosas visibles (nódulos, úlceras, cambios de coloración sospechosos) en la línea Z, las cuales deben ser biopsiadas de forma dirigida para descartar displasia o neoplasia
- Un examen endoscópico cuidadoso y de alta calidad con identificación precisa de los puntos de referencia (margen proximal de los pliegues gástricos, pinza diafragmática y unión escamocolumnar) es esencial para distinguir correctamente entre una línea Z irregular y un verdadero Barrett de segmento corto
Los pacientes con línea Z irregular sin lesiones visibles no deben ser biopsiados ni incluidos en programas de vigilancia endoscópica
Una línea Z irregular no es sinónimo de esófago de Barrett. La línea Z irregular se define como una unión escamocolumnar de aspecto irregular con lengüetas de mucosa columnar que se extienden <1 cm por encima de la unión gastroesofágica (UGE), y se observa en aproximadamente el 10-15% de las endoscopias digestivas altas, con un 44% de estas mostrando metaplasia intestinal (MI) en biopsias.
Sin embargo, la ACG establece que para diagnosticar esófago de Barrett se requiere mucosa columnar de al menos 1 cm de longitud por encima de la UGE con MI confirmada histológicamente.
La principal conclusión de la evidencia disponible es que la línea Z irregular aislada (mucosa columnar <1 cm por encima de la UGE) tiene un riesgo de progresión a displasia de alto grado o adenocarcinoma esofágico prácticamente nulo, y las complicaciones clínicas asociadas son mínimas desde el punto de vista oncológico, pero significativas desde el punto de vista iatrogénico
Manejo del Esofago de Barrett
Seguimiento del esofago de Barrett
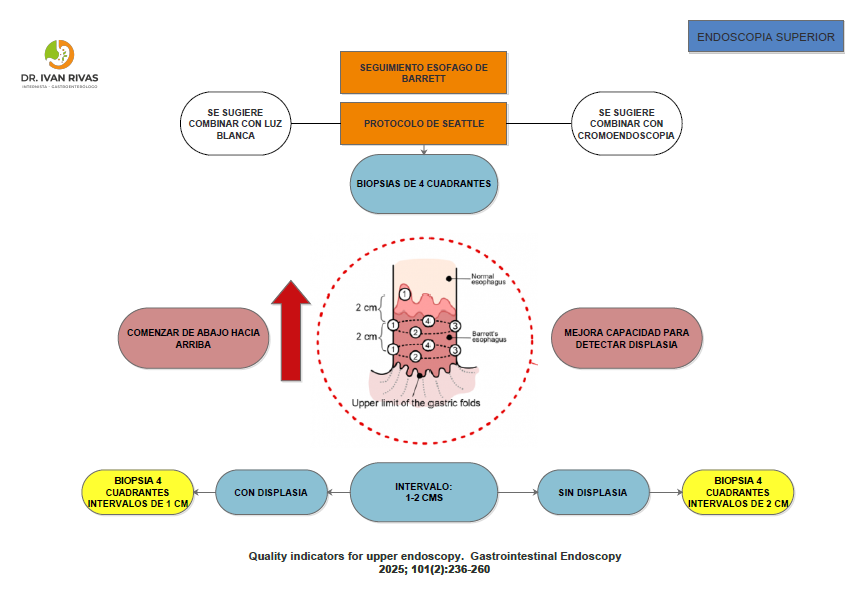
- La AGA y ACG recomiendan un seguimiento endoscópico estructurado del esófago de Barrett basado en el grado de displasia y la longitud del segmento, utilizando el protocolo de biopsias de Seattle como estándar de muestreo
- Barrett no displásico (NDBE) 3 cm: Vigilancia cada 5 años
- Barrett no displásico (NDBE) ≥3 cm: Vigilancia cada 3 años
- Displasia de bajo grado (DBG) confirmada: Vigilancia cada 6-12 meses (o considerar terapia de erradicación endoscópica)
- Displasia de alto grado (DAG): Terapia de erradicación endoscópica (no vigilancia)
Las guías actuales de la ACG (2022) y AGA (2025) establecen que no es necesario repetir la endoscopia al año del diagnóstico inicial de Barrett no displásico, como se recomendaba previamente, dado que no hay evidencia de que un intervalo tan corto mejore el pronóstico
Manejo endoscopico del esofago de Barrett
Recomendaciones previas a terapia de erradicación endoscópica
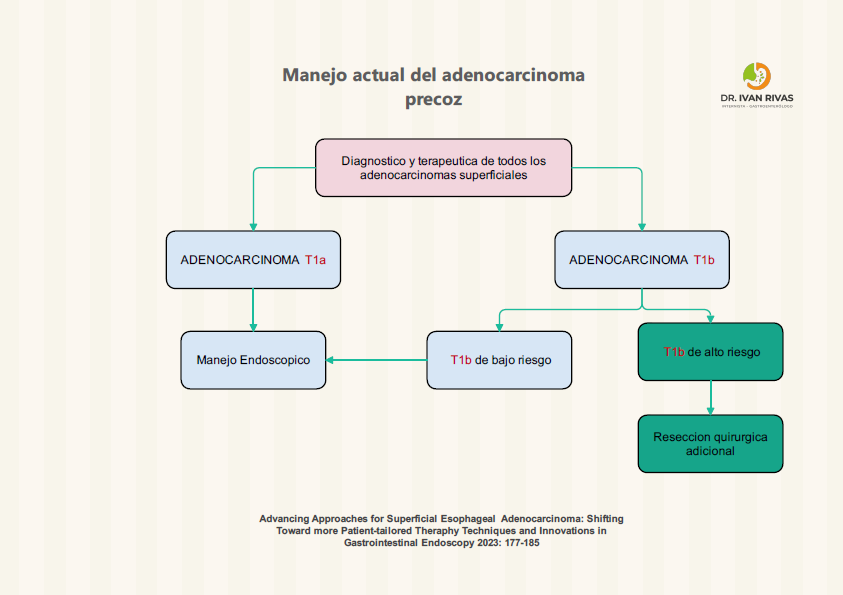
Terapia de erradicación endoscópica
Terapia de erradicación endoscópica de acuerdo al grado de invasión
Terapia de erradicación endoscópica (TEE)
Resección mucosal endoscópica (RME) en Esofago de Barrett

Efectividad de la RME en esofago de Barrett
RME convencional
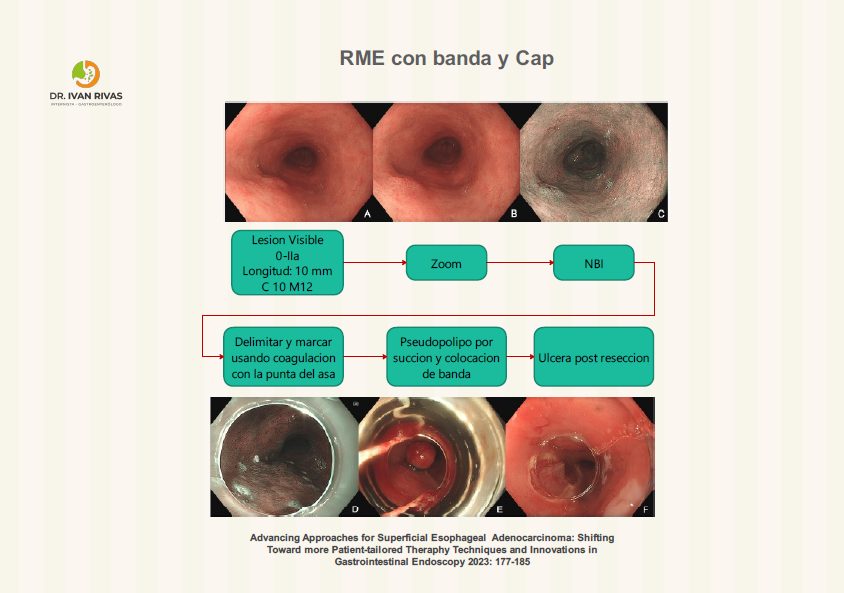
Resección mucosal endoscópica modificada
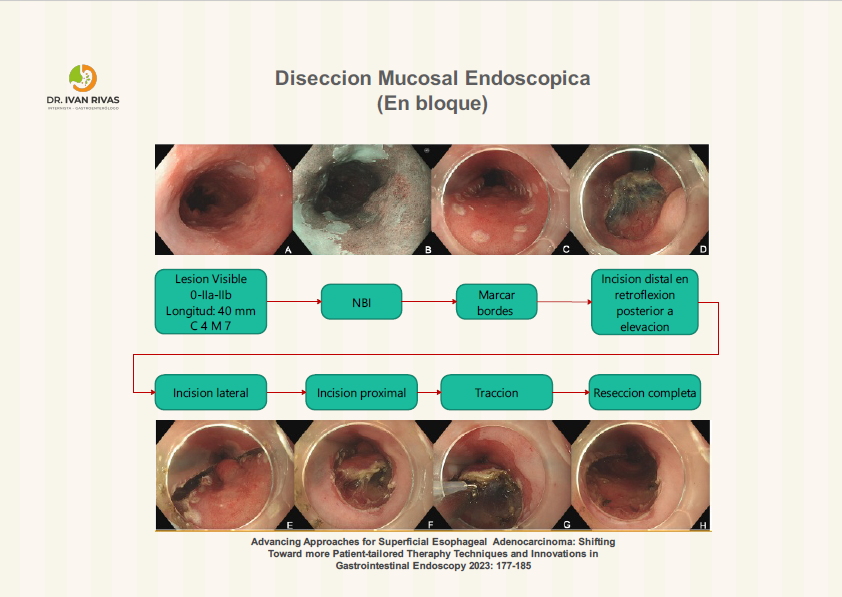
Disección Mucosal Endoscópica (Mucosectomia)

Radiofrecuencia (RFA)
La radiofrecuencia (RFA) es el método endoscópico más establecido para la erradicación de la mucosa de Barrett con displasia, y su uso se fundamenta en principios técnicos, clínicos y de seguridad que han sido definidos en la literatura médica reciente y en guías de práctica clínica
Los principios fundamentales del uso de la RFA para el tratamiento del esófago de Barrett incluyen:
- Selección adecuada del paciente y evaluación previa: La RFA está indicada principalmente en pacientes con esófago de Barrett con displasia confirmada (bajo o alto grado) o cáncer precoz, tras la resección endoscópica de lesiones visibles. La mucosa debe ser plana, sin ulceraciones ni exudados, ya que la presencia de inflamación o erosiones puede aumentar el grosor de la mucosa y reducir la eficacia de la ablación, además de dificultar la detección de lesiones neoplásicas subyacentes
- Inspección endoscópica cuidadosa: Antes de cada sesión de RFA, se debe realizar una inspección detallada con endoscopia de alta definición y, preferentemente, cromoendoscopia óptica para descartar lesiones visibles que requieran resección endoscópica en lugar de ablación
- Regímenes de energía y dispositivos: Existen dos modalidades principales: ablación circunferencial (usando un catéter balón, como HALO360) y ablación focal (usando dispositivos como HALO90). Los regímenes de energía varían según el protocolo y la región: en EE.UU. se emplea típicamente 2 × 2 × 12 J/cm², mientras que en Europa se utiliza 2 × 2 × 15 J/cm², ambos con limpieza intermedia del coagulum para optimizar la transferencia de energía. En regímenes simplificados, se han evaluado tres aplicaciones sucesivas de 12 J/cm² sin limpieza intermedia
- Sesiones repetidas y seguimiento: La RFA se realiza en sesiones programadas cada 2-3 meses, permitiendo la cicatrización y regeneración del epitelio escamoso. El tratamiento puede extenderse durante más de un año, y se repite hasta lograr la erradicación endoscópica e histológica del Barrett
- Control de la acidez gástrica: Es imprescindible el uso de inhibidores de la bomba de protones a dosis doble durante todo el tratamiento para favorecer la cicatrización y prevenir la recurrencia. En algunos estudios europeos se añade un antagonista H2 y sucralfato por corto tiempo tras cada sesión, aunque no existen estudios comparativos robustos sobre el régimen óptimo
- Evitar biopsias en mucosa inflamada: No se recomienda tomar biopsias en mucosa con signos de inflamación o cicatrización incompleta, ya que los cambios reactivos pueden dificultar la interpretación histológica y la sangre puede interferir con la transferencia de energía
- Manejo de complicaciones: Las complicaciones más frecuentes son las estenosis esofágicas, que suelen resolverse con dilatación endoscópica. El riesgo de complicaciones aumenta con la longitud del Barrett y la presencia de displasia de alto grado o cáncer precoz
- Resultados y eficacia: La RFA ha demostrado una alta tasa de erradicación de la displasia y la metaplasia intestinal, y reduce significativamente el riesgo de progresión a adenocarcinoma en comparación con la vigilancia endoscópica
Principios
- La radiofrecuencia utilizada en el tratamiento endoscópico de lesiones del tracto digestivo se basa en la aplicación de corriente alterna de alta frecuencia (300 kHz–3 MHz) a través de electrodos, lo que genera un campo eléctrico en el tejido objetivo. Este campo provoca desplazamiento de moléculas y fricción iónica, resultando en calentamiento local por pérdida dieléctrica, que induce necrosis por coagulación y desnaturalización de proteínas celulares
- El grado de lesión térmica depende de la potencia aplicada, la duración, el tipo de electrodo y el contacto con el tejido, así como de la conductividad térmica y la perfusión sanguínea local, que pueden disipar el calor y limitar la extensión de la ablación
- En sistemas endoscópicos, la configuración del electrodo (monopolar o bipolar) y el tamaño relativo de los electrodos determinan la densidad de corriente y, por tanto, la temperatura alcanzada en el tejido. Electrodos pequeños concentran la energía y producen mayor calentamiento local, mientras que electrodos de mayor superficie dispersan la energía y minimizan el daño colateral
- Los dispositivos modernos suelen incorporar sensores de temperatura y sistemas de irrigación para controlar la temperatura y la impedancia, evitando la desecación excesiva del tejido (>110°C), que puede actuar como aislante y reducir la eficacia de la ablación
- La relación entre potencia y profundidad de ablación es lineal: a mayor potencia, mayor profundidad y extensión de la lesión, como se ha demostrado en modelos animales y en aplicaciones clínicas en esófago, estómago y vía biliar
- Además, la irrigación durante la ablación permite crear lesiones más profundas y extensas a temperaturas más bajas, lo que reduce el riesgo de perforación y daño térmico excesivo
En resumen, los principios físicos fundamentales de la radiofrecuencia endoscópica en el tracto digestivo incluyen la generación de calor por corriente alterna de alta frecuencia, la modulación de la densidad de corriente mediante el diseño del electrodo, el control de temperatura y la influencia de la perfusión tisular, todo orientado a lograr necrosis controlada y segura del tejido objetivo
Tipos de sonda de radiofrecuencia
Para el tratamiento endoscópico del esófago de Barrett mediante radiofrecuencia, existen dos tipos principales de sondas de ablación, cada una diseñada para abordar diferentes patrones de mucosa y extensión de la enfermedad:
Sonda de ablación circunferencial (balón)
- El catéter de balón circunferencial, como el HALO360 o el 360 Express, está indicado para la ablación de segmentos extensos de mucosa de Barrett (habitualmente ≥3 cm). Este dispositivo consiste en un balón que se infla dentro del esófago, permitiendo el contacto uniforme de los electrodos con la mucosa y la aplicación de energía de manera circunferencial. El 360 Express es una versión autoajustable que elimina la necesidad de medición previa del diámetro esofágico, optimizando el contacto y reduciendo el tiempo del procedimiento
- El régimen estándar de ablación con estos dispositivos suele ser “one-clean-one” (una aplicación, limpieza, segunda aplicación) para minimizar el riesgo de estenosis y maximizar la eficacia
Sonda de ablación focal (endoscópica)
- El catéter focal, como el HALO90, se monta en el extremo del endoscopio y está diseñado para tratar áreas residuales de Barrett, segmentos cortos (<3 cm), islotes, lenguas, o la unión esofagogástrica
- Permite la aplicación dirigida de energía sobre áreas específicas, especialmente útiles tras la ablación circunferencial inicial o para lesiones persistentes. El régimen de energía puede variar, pero los protocolos más utilizados incluyen dos aplicaciones, limpieza, y dos aplicaciones adicionales (“two-clean-two”), aunque existen regímenes simplificados con tres aplicaciones sucesivas sin limpieza intermedia
La elección entre sonda circunferencial o focal depende de la extensión y morfología de la mucosa de Barrett, así como de la presencia de lesiones residuales tras la resección endoscópica
Procedimiento para Radiofrecuencia
La aplicación de la ablación por radiofrecuencia endoscópica en el esófago de Barrett sigue un protocolo estandarizado, basado en la evidencia y consensos internacionales. Los pasos principales son:
- Evaluación previa y selección del paciente: Se realiza endoscopia de alta resolución, preferentemente con cromoendoscopia óptica, para identificar la extensión del esófago de Barrett y descartar lesiones visibles o neoplasia invasiva. Si existen lesiones nodulares o sospechosas, se indica resección endoscópica antes de la ablación
- Preparación y sedación: El procedimiento se realiza en régimen ambulatorio bajo sedación consciente (midazolam, propofol, o combinación con opioides)
- Selección del dispositivo: Se elige el tipo de sonda según la extensión de la mucosa de Barrett: sonda circunferencial (balón) para segmentos largos (≥3 cm) y sonda focal para áreas residuales, cortas o islotes
- Control de la mucosa y repetición de sesiones: Las sesiones de ablación se programan cada 2-3 meses, permitiendo la cicatrización y regeneración escamosa. Solo se repite la ablación cuando la mucosa residual está plana y sin ulceración; si hay esofagitis o ulceración, se pospone el tratamiento y se optimiza la terapia antisecretora
- Terapia farmacológica adyuvante: Se indica inhibidor de la bomba de protones a dosis doble durante todo el tratamiento, y se puede añadir antagonista H2 y sucralfato por 2 semanas tras cada sesión, según protocolos europeos
- Seguimiento endoscópico y biopsias: Tras la erradicación endoscópica, se realiza endoscopia de control a los 3 meses y luego anualmente. Se toman biopsias en cuatro cuadrantes cada 2 cm sobre la extensión original del Barrett y en la unión esofagogástrica para confirmar la erradicación histológica
- Manejo de lesiones residuales: Si persisten islotes (<5 mm), se puede emplear coagulación con plasma de argón; si hay áreas mayores, se indica resección endoscópica
- Vigilancia de complicaciones: Las complicaciones más frecuentes son estenosis esofágica, dolor, y, raramente, sangrado o perforación. La estenosis se maneja endoscópicamente
Ablación circunferencial
- Se mide el diámetro esofágico y se coloca el catéter de balón
- Se aplica energía predeterminada (por ejemplo, 12 J/cm² y 40 W/cm²)
- Se retira el catéter, se limpia el área de coagulum, y se repite la ablación (“one-clean-one”)
- Para segmentos largos, se reposiciona el catéter en incrementos de 3 cm
Ablación focal
- Se utiliza el catéter focal (HALO90/Barrx90)
- Se aplican dos ablaciones, se limpia el área y el electrodo, y se realizan dos ablaciones adicionales (“two-clean-two”). Alternativamente, se puede emplear un régimen simplificado de tres aplicaciones sucesivas sin limpieza intermedia
- La unión esofagogástrica se ablaciona siempre de forma circunferencial, independientemente de su apariencia
Tips a tener en cuenta
- La inspección endoscópica inicial debe ser meticulosa, utilizando endoscopios de alta resolución y preferentemente cromoendoscopia óptica, para descartar lesiones visibles o nodulares. Toda lesión visible debe ser resecada mediante mucosectomía antes de la ablación; la RFA está indicada solo en mucosa plana
- La RFA debe realizarse en mucosa de Barrett sin signos de inflamación, exudado o ulceración. Si existe esofagitis o cicatrización incompleta, la ablación debe posponerse al menos 6 semanas y optimizarse la terapia antisecretora. No se recomienda tomar biopsias en mucosa inflamada, ya que la diferenciación histológica entre cambios reactivos y displasia es difícil y puede interferir con la transferencia de energía
- La elección del dispositivo depende de la extensión: el catéter circunferencial (balón) se utiliza para segmentos largos (≥3 cm), aplicando energía en incrementos de 3 cm, mientras que el catéter focal se emplea para áreas residuales, cortas o la unión esofagogástrica, que debe ser tratada siempre de forma circunferencial, independientemente de su apariencia
- Los regímenes de ablación focal más utilizados incluyen el estándar (dos aplicaciones, limpieza, dos aplicaciones adicionales) y el simplificado (tres aplicaciones sucesivas sin limpieza intermedia), ambos con resultados comparables en eficacia y seguridad
- Las sesiones de RFA deben espaciarse cada 2-3 meses, permitiendo la cicatrización y regeneración escamosa. La ablación solo debe repetirse cuando la mucosa residual esté plana y sin ulceración
- Es fundamental mantener una terapia antisecretora óptima durante todo el tratamiento, habitualmente con inhibidor de bomba de protones a dosis doble. En Europa, se suele añadir antagonista H2 y sucralfato por 2 semanas tras cada sesión, aunque no existen estudios comparativos robustos sobre el régimen óptimo
- El seguimiento endoscópico incluye biopsias en cuatro cuadrantes cada 2 cm sobre la extensión original del Barrett y en la unión esofagogástrica, para confirmar la erradicación histológica
- Si persisten islotes de Barrett menores de 5 mm, se puede emplear coagulación con plasma de argón; si hay áreas mayores, se recomienda resección endoscópica
- Las complicaciones más frecuentes son dolor torácico, estenosis esofágica y, raramente, sangrado o perforación. La estenosis se maneja con dilatación endoscópica
- El peor desenlace es no reconocer un cáncer invasivo durante el tratamiento; por ello, cada sesión debe iniciar con una inspección cuidadosa para descartar progresión neoplásica
Crioterapia
Principios de la Crioterapia
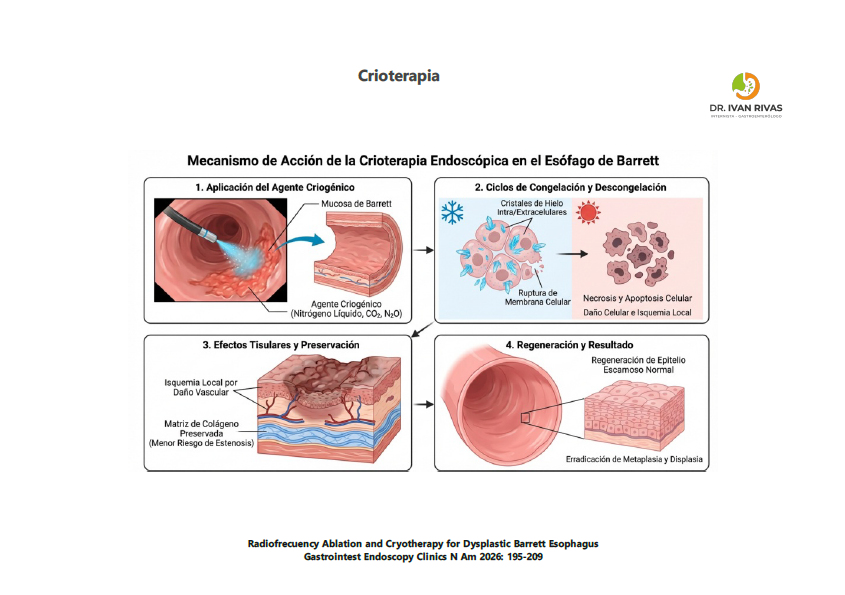
- La crioterapia endoscópica actúa sobre la mucosa esofágica y el epitelio metaplásico del esófago de Barrett mediante la aplicación de un agente criogénico (nitrógeno líquido, dióxido de carbono o óxido nitroso) que produce ciclos rápidos de congelación y descongelación. Este proceso genera daño celular por varios mecanismos: ruptura de membranas celulares, formación de cristales de hielo intra y extracelular, y alteración de la homeostasis celular, lo que induce necrosis y apoptosis de las células metaplásicas y displásicas
- Además, la crioterapia provoca daño vascular local, generando isquemia tisular que contribuye a la destrucción de la mucosa patológica
- A diferencia de otras técnicas térmicas como la radiofrecuencia, la crioterapia preserva la matriz de colágeno y la arquitectura tisular, lo que favorece una cicatrización más fisiológica y reduce el riesgo de estenosis
- El resultado es la erradicación selectiva de la mucosa metaplásica y displásica, permitiendo la regeneración de epitelio escamoso normal
Modalidades de crioterapia
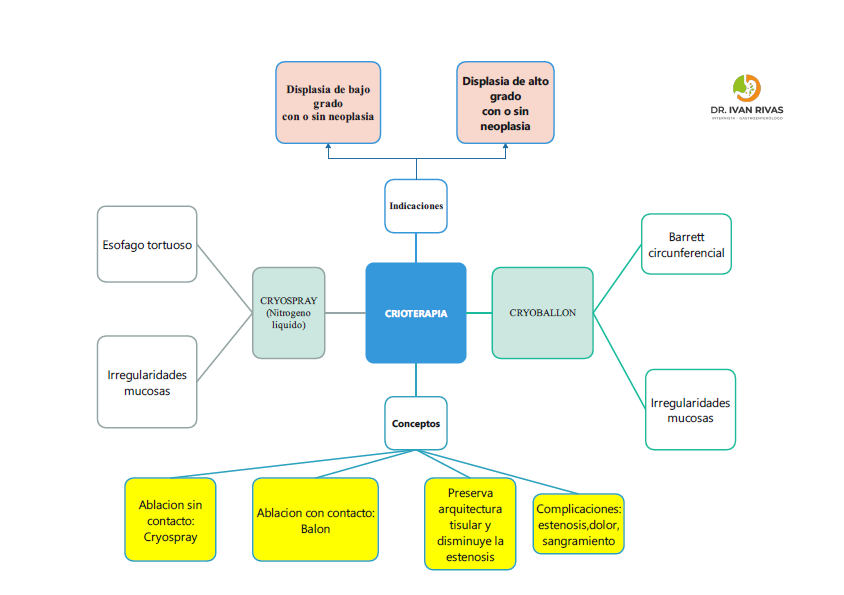
Actualmente existen dos modalidades principales de crioterapia endoscópica para el tratamiento del esófago de Barrett: la crioterapia por spray y la crioterapia con balón de contacto (cryoballoon). Ambas están aprobadas por la FDA para uso en el tracto gastrointestinal en Estados Unidos.
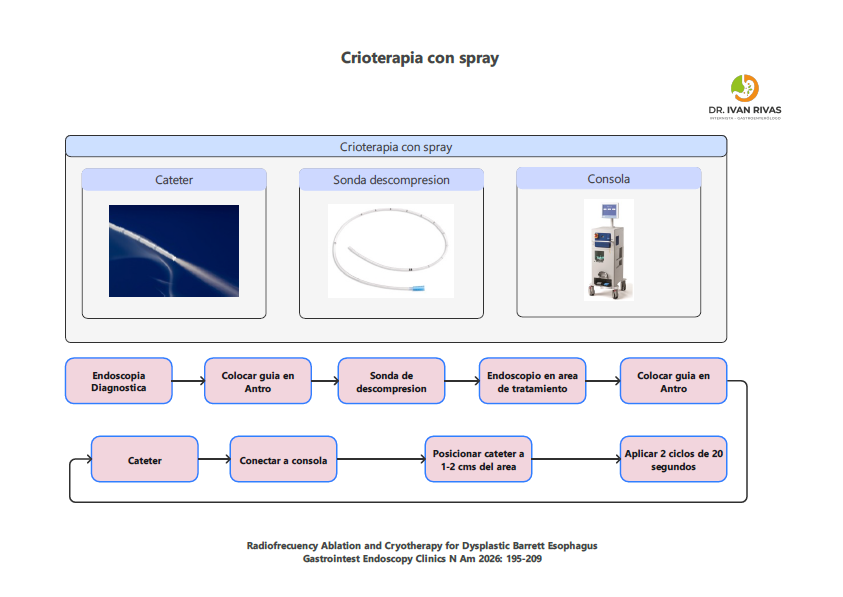
La crioterapia por spray utiliza un catéter flexible para aplicar un agente criogénico, típicamente nitrógeno líquido, directamente sobre la mucosa esofágica a través del canal de trabajo del endoscopio. Este método requiere la colocación de un tubo de descompresión para manejar la expansión del gas durante la aplicación. El sistema más utilizado es el truFreeze (STERIS, Mentor, OH).
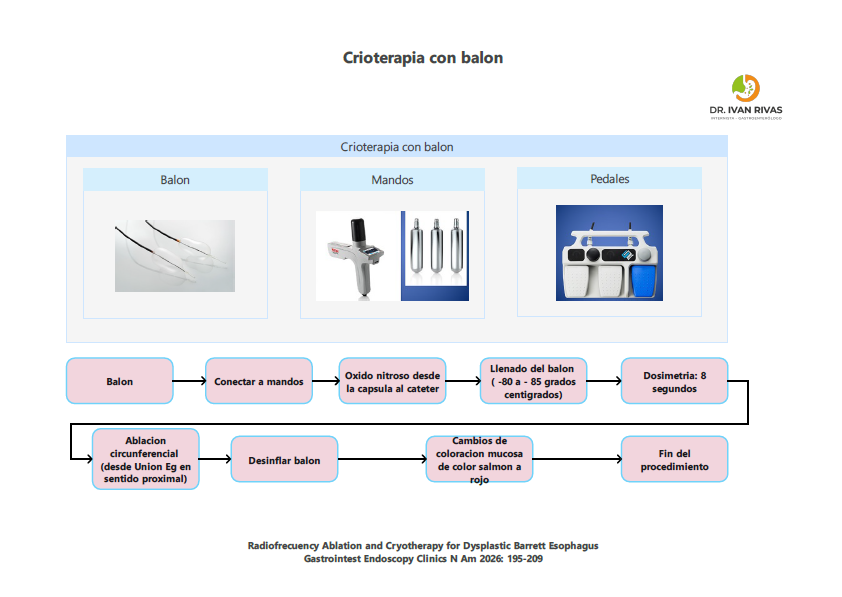
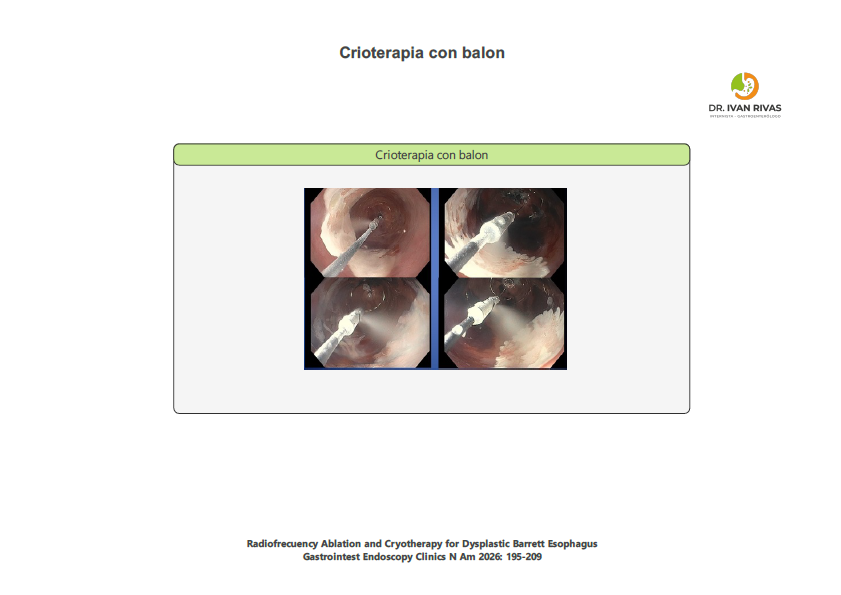
La crioterapia con balón de contacto emplea un sistema de balón inflable que se posiciona sobre la mucosa y libera óxido nitroso, generando congelación focal y controlada. El dispositivo más representativo es el C2 CryoBalloon Ablation System (Merit Medical), que permite una aplicación rotatoria y precisa del criógeno. Esta modalidad se caracteriza por su facilidad de uso y menor dispersión del agente criogénico.
Ambas técnicas han demostrado eficacia y seguridad en la erradicación de displasia y metaplasia intestinal asociada a esófago de Barrett, tanto en pacientes naïve como en aquellos refractarios a radiofrecuencia
Crioterapia con spray
Crioterapia con balón
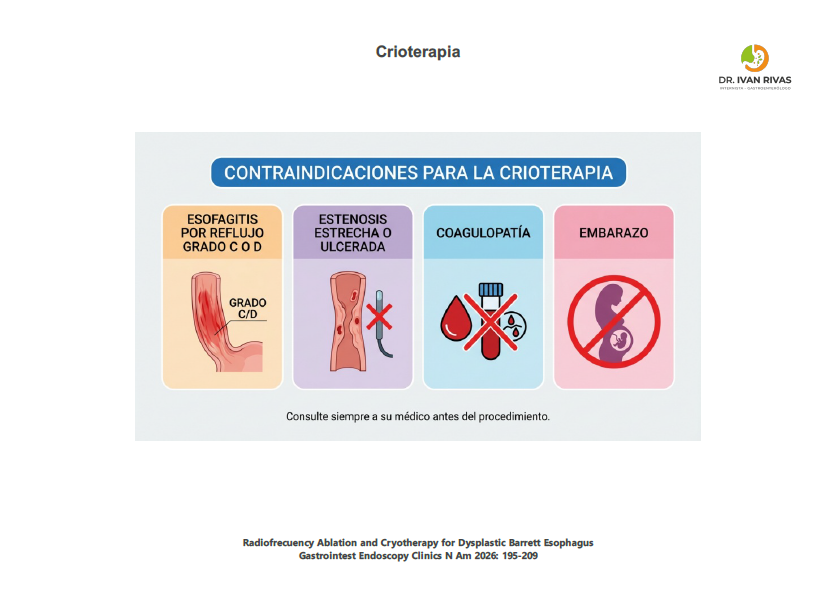
Contraindicaciones para la Crioterapia
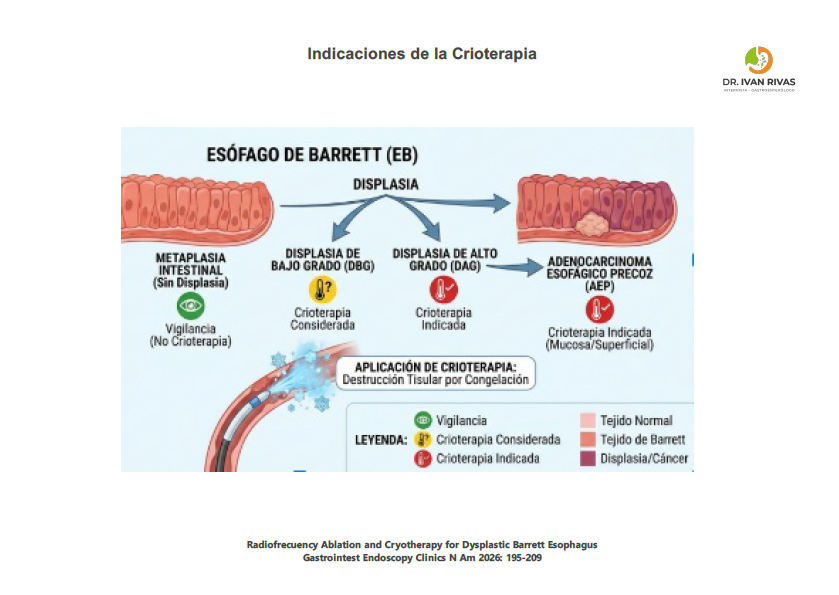
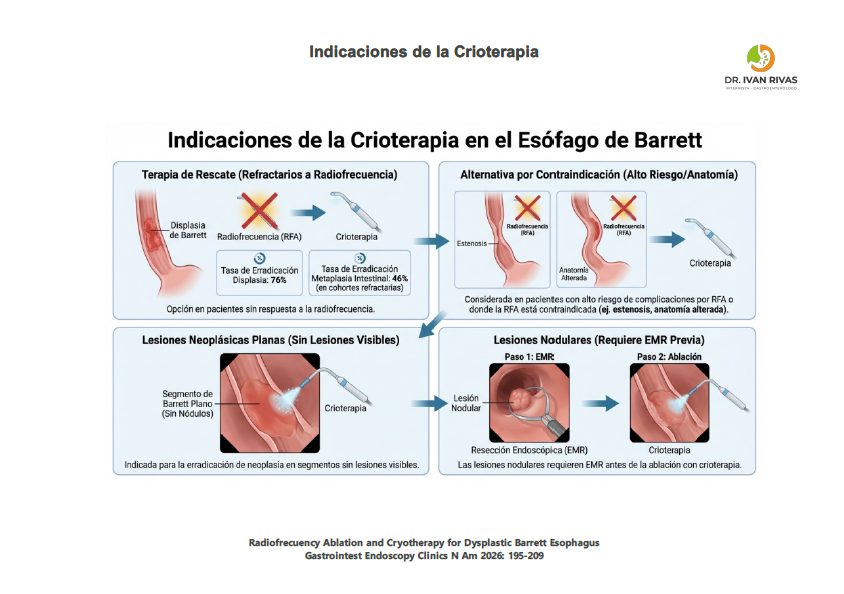
Indicaciones para la crioterapia
- La crioterapia está indicada principalmente en esófago de Barrett con displasia de bajo o alto grado, y adenocarcinoma intramucoso. Es especialmente relevante en pacientes que no son candidatos a radiofrecuencia o que han presentado fracaso o contraindicación a otras técnicas ablativas. No se recomienda en Barrett no displásico, salvo situaciones excepcionales donde el riesgo de progresión sea elevado
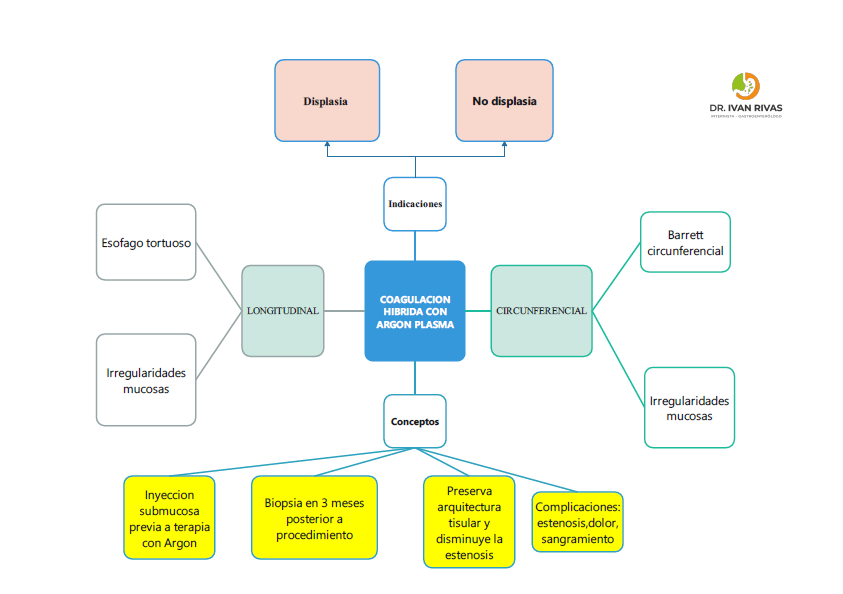
Terapia con Argón Plasma Híbrido
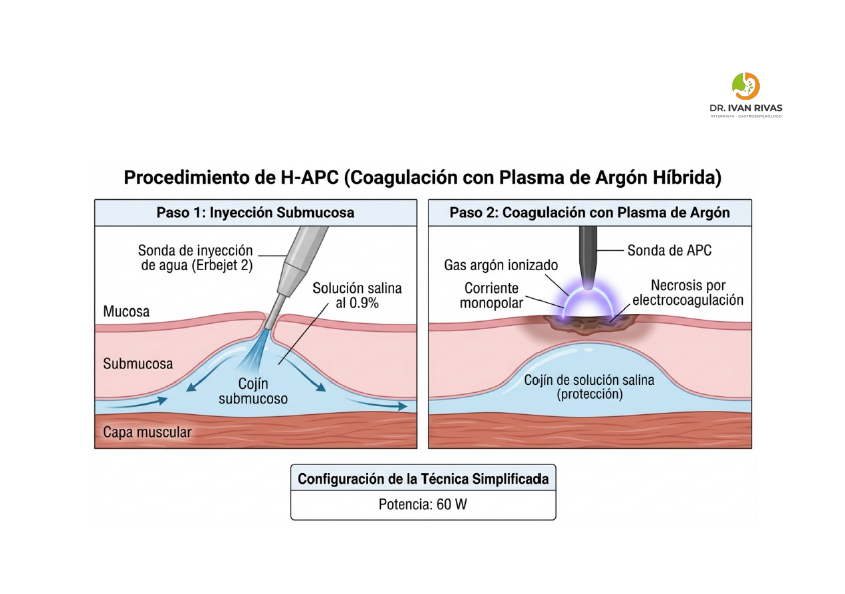
La coagulación híbrida con plasma de argón (H-APC) es una técnica ablativa térmica que combina la inyección submucosa de solución salina con la coagulación con plasma de argón convencional. Esta técnica se desarrolló con el objetivo de reducir las complicaciones, particularmente la formación de estenosis, al crear un “colchón” protector submucoso antes de la ablación.
Mecanismo y técnica:
La H-APC utiliza una sonda de inyección de agua (Erbejet 2) para realizar inyección submucosa de solución salina al 0.9% antes de aplicar la coagulación con plasma de argón. El gas argón ionizado conduce una corriente monopolar al tejido, causando necrosis por electrocoagulación. La técnica simplificada utiliza una potencia de 60W
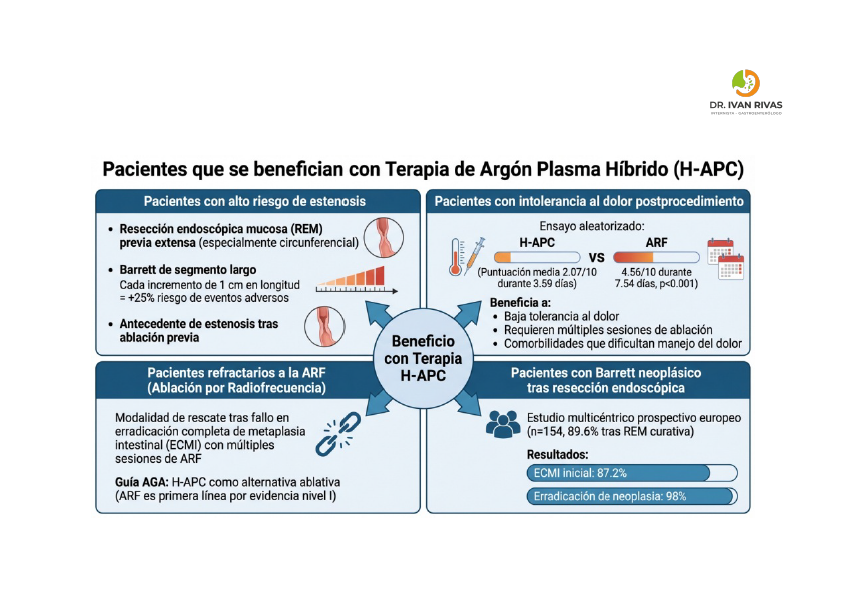
La guía de actualización de práctica clínica de la AGA de 2020 menciona la H-APC entre las modalidades ablativas estudiadas, pero señala que la ARF sigue siendo la terapia de primera línea debido a la evidencia de nivel I que documenta su superioridad sobre la vigilancia endoscópica. La guía indica que “debido a la escasez de datos comparativos directos entre modalidades ablativas alternativas, el uso más apropiado de estas modalidades en los algoritmos de tratamiento aún está por determinarse”
Uso en Barrett refractario:
La H-APC puede considerarse como modalidad alternativa en pacientes que no responden a la ARF, particularmente en aquellos con alto riesgo de estenosis o que han experimentado dolor significativo con la ARF
Manejo de displasia y cancer en esofago de Barrett
Displasia de bajo grado
Manejo de la displasia de alto grado en esofago de Barrett
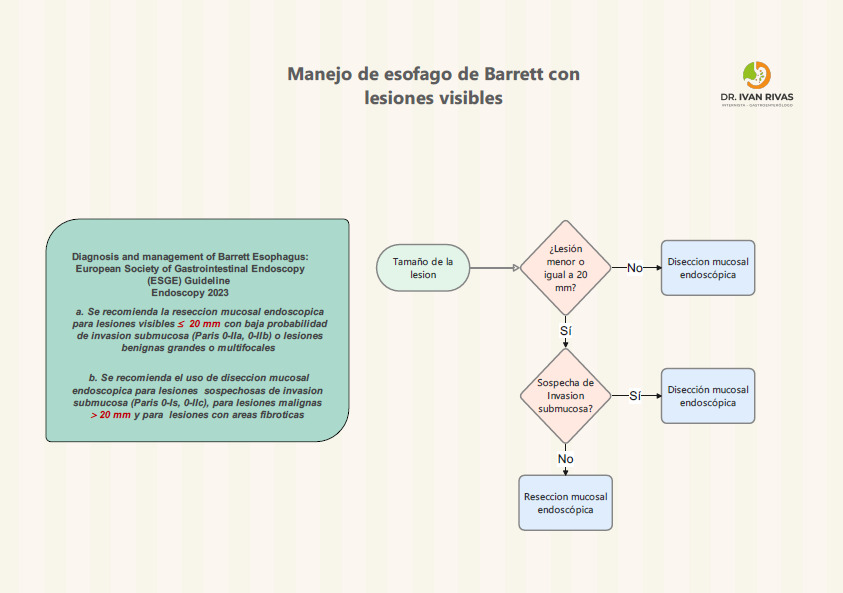
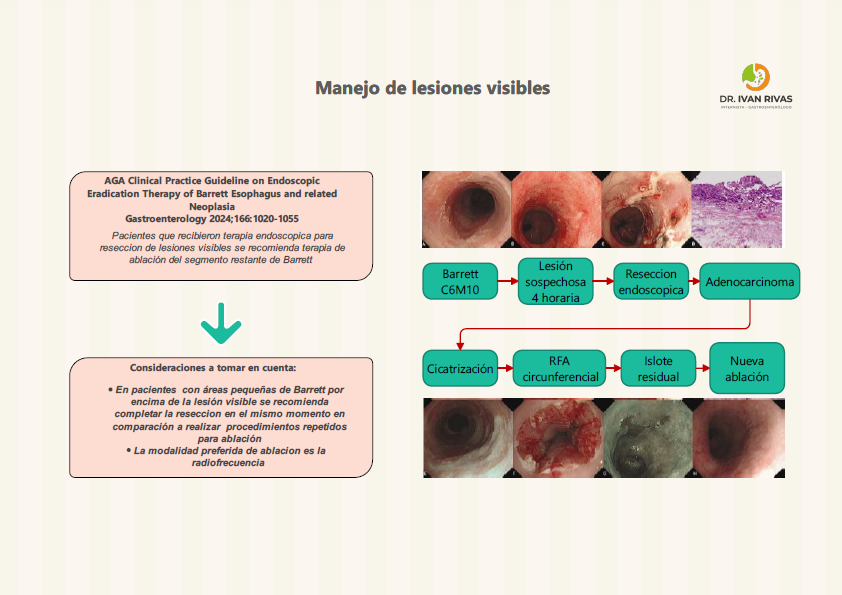
Manejo de lesiones visibles en esofago de Barrett
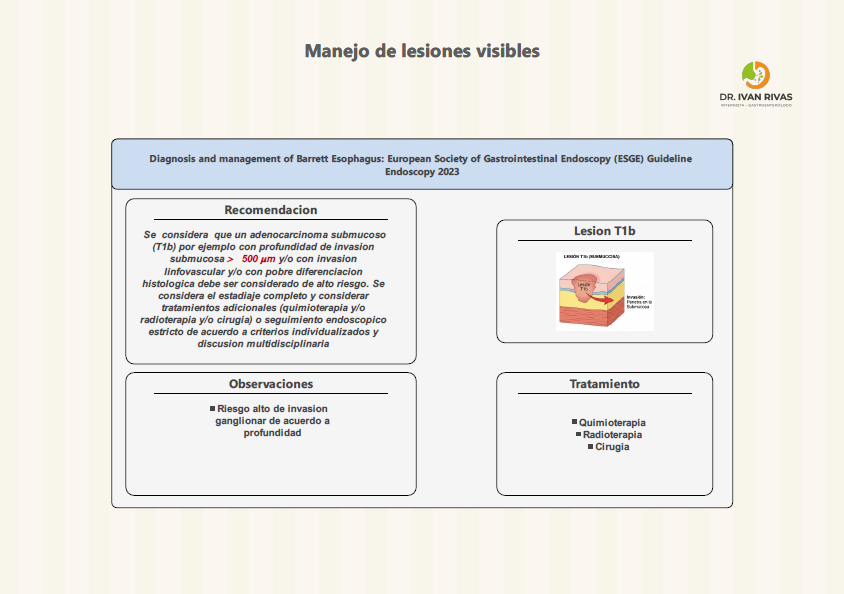
Esofago de Barrett refractario
Definición de Barrett refractario
No existe una definición formal universalmente aceptada de “esófago de Barrett refractario” en las guías de práctica clínica principales (ACG, AGA). Sin embargo, el término se utiliza en la literatura para describir dos escenarios clínicos principales:
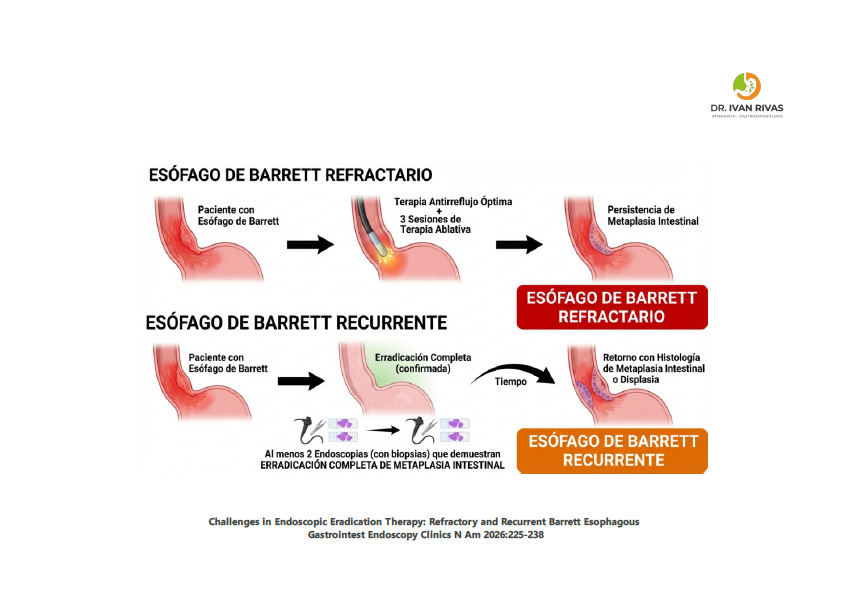
Barrett refractario a la terapia de erradicación endoscópica (TEE):
Este es el uso más frecuente del término y se refiere a la persistencia de metaplasia intestinal y/o displasia a pesar de múltiples sesiones de ablación por radiofrecuencia (ARF). Un estudio multicéntrico del consorcio TREAT-BE propuso un umbral operativo: la media de sesiones necesarias para lograr la erradicación completa de la metaplasia intestinal (ECMI) es de 2.9 sesiones (mediana de 2), y tras 3 sesiones, el 73% de los pacientes logran la ECMI. Los autores concluyeron que se deben considerar terapias alternativas y pruebas diagnósticas adicionales en pacientes que no tienen una respuesta significativa a la TEE después de 3 sesiones. De forma similar, un estudio australiano definió operativamente a los “respondedores pobres” como aquellos pacientes que requirieron 4 o más sesiones de tratamiento para lograr la erradicación, encontrando que el 18% de los pacientes cayeron en esta categoría
Barrett refractario al tratamiento médico (reflujo refractario):
Se refiere a la persistencia de reflujo gastroesofágico a pesar de la terapia con IBP optimizada, lo cual impide la regeneración escamosa adecuada y contribuye al fracaso de la TEE. La guía de la AGA de 2024 enfatiza que el fracaso en lograr la ECMI debe llevar a una reevaluación y optimización del control del reflujo, incluyendo monitorización ambulatoria del reflujo y consideración de funduplicatura
Consideraciones importantes:
La guía de la AGA (actualización de práctica clínica de 2020) señala que las sesiones de ablación se programan cada 2-3 meses hasta lograr la erradicación completa, y que cada sesión debe comenzar con una inspección endoscópica cuidadosa para excluir lesiones visibles que requieren resección en lugar de ablación. Si hay esofagitis erosiva o ulceración, la ablación debe posponerse y se debe verificar la supresión ácida adecuada.
En resumen, aunque no existe una definición estandarizada, el concepto de Barrett refractario se aplica pragmáticamente cuando no se logra la ECMI tras aproximadamente 3 sesiones de TEE adecuadamente realizadas, lo que debe llevar a reevaluar el control del reflujo y considerar modalidades ablativas alternativas
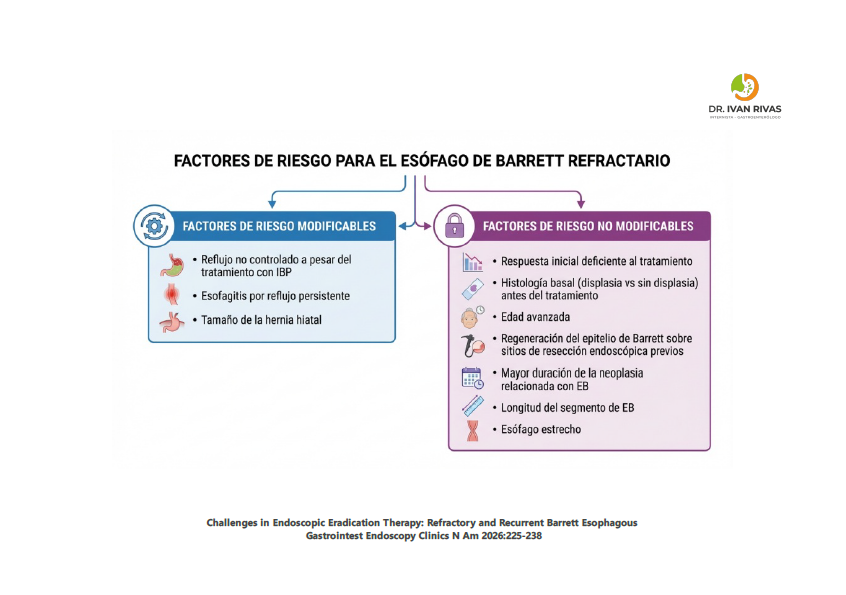
Factores de riesgo para esofago de Barrett refractario
Los factores de riesgo para esófago de Barrett refractario (fracaso en lograr la erradicación completa de la metaplasia intestinal [ECMI] o recurrencia tras la terapia de erradicación endoscópica [TEE]) se pueden clasificar en factores relacionados con el paciente, la enfermedad, el reflujo y el procedimiento.
Factores relacionados con el reflujo (los más importantes)
El reflujo gastroesofágico mal controlado es el factor más frecuentemente asociado con el fracaso de la TEE. En un estudio unicéntrico, el 41% de los fracasos se debieron a falta de adherencia a la dosificación de IBP dos veces al día con horario adecuado. Los pacientes con Barrett tienen mayor reflujo que otros pacientes con ERGE, frecuentemente con reflujo nocturno severo que puede persistir con IBP una vez al día, y a menudo eventos de reflujo asintomáticos. La presencia de síntomas de reflujo persistentes se asoció fuertemente con recurrencia.
Factores anatómicos
- Hernia hiatal: Es un predictor significativo de recurrencia (OR ajustado 13.8 en un estudio multicéntrico prospectivo). Pacientes con hernias hiatales más grandes (mediana de 7 cm) tuvieron mayor probabilidad de no cicatrización tras la ablación inicial. La ausencia de hernia hiatal fue el factor más importante asociado con la regresión del Barrett. El tamaño de la hernia hiatal también se asoció con recurrencia de displasia
- Barrett de segmento largo: Se asoció con mayor riesgo de recurrencia (HR 1.59; IC 95% 1.01-2.51) y con fracaso de la ablación (mediana de segmento columnar de 8.5 cm en fracasos vs. 3 cm en éxitos, p=0.002)
Factores histológicos
- Displasia de alto grado (DAG) o carcinoma intramucoso previo a la ablación se asoció con mayor riesgo de recurrencia comparado con displasia de bajo grado (OR ajustado 4.19; HR 1.71). La tasa de incidencia de recurrencia fue de 13.5 por 100 personas-año en pacientes con DAG basal vs. 8.3 en displasia de bajo grado
Factores relacionados con el procedimiento
- Monoterapia con ARF (sin resección endoscópica mucosa combinada) se asoció con mayor riesgo de recurrencia de cualquier Barrett (OR 3.0), recurrencia displásica (RRR 5.53) y recurrencia tardía (RRR 3.24), mientras que la combinación de REM + ARF redujo el riesgo de recurrencia displásica (RRR 0.27)
- Centros de bajo volumen (<3 procedimientos de ablación anuales) se asociaron con mayor riesgo de recurrencia comparados con centros de alto volumen (>10 procedimientos anuales; HR 0.19)
- Mayor número de sesiones requeridas para lograr la ECMI se asoció con recurrencia (OR ajustado 1.8)
Otros factores:
Edad avanzada, tabaquismo, obesidad, raza no blanca y presencia de esofagitis erosiva también se han reportado como factores de riesgo, aunque con evidencia más limitada
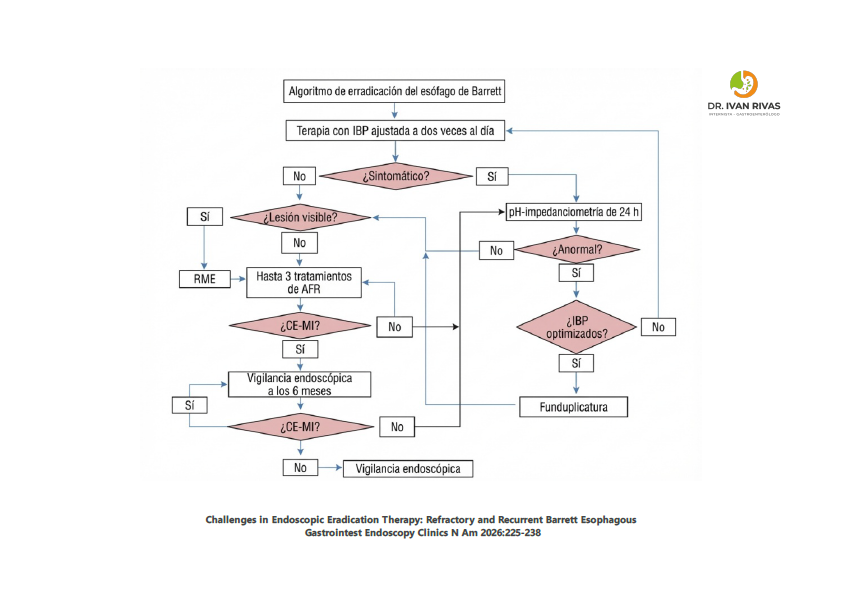
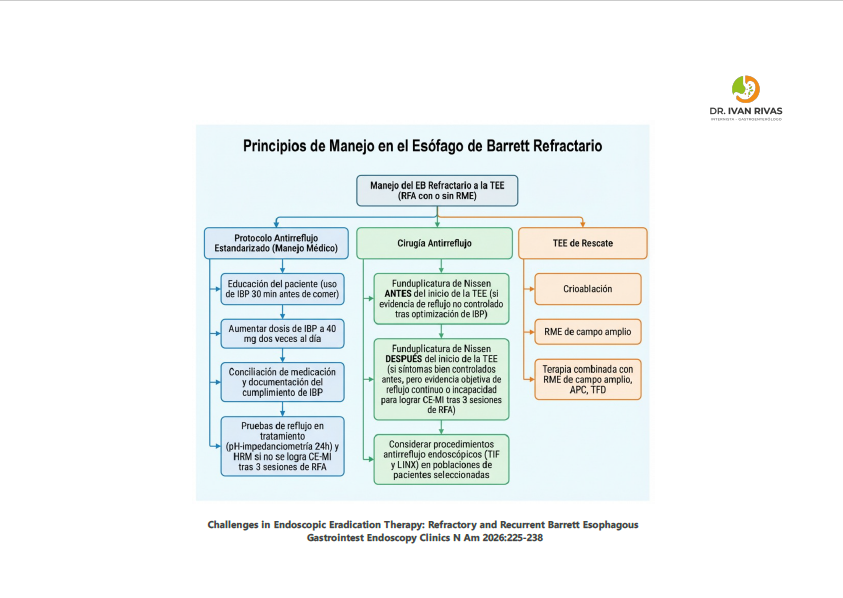
Manejo del esofago de Barrett refractario
Según la guía de práctica clínica de la AGA de 2024, el pilar del manejo es la optimización del control del reflujo. En un estudio unicéntrico, el fracaso en lograr la ECMI se asoció más frecuentemente con reflujo mal controlado, y el 41% de los casos se debió a falta de adherencia a la dosificación de IBP dos veces al día con horario adecuado (30-45 minutos antes de las comidas).
Tras la optimización del control del reflujo mediante reeducación, cambio a un IBP más potente o funduplicatura, el 94% de los pacientes que inicialmente no lograron la ECMI finalmente la alcanzaron.
Las estrategias específicas incluyen:
- IBP dos veces al día con horario adecuado (30-45 minutos antes de las comidas)
- Evitar comer 4 horas antes de acostarse y elevar la cabecera de la cama para minimizar el reflujo nocturno
- Monitorización ambulatoria del reflujo para guiar decisiones, incluyendo la derivación para funduplicatura antes de reanudar la TEE
- Los bloqueadores competitivos de ácido potásico (PCABs) podrían tener un papel útil, aunque se requieren más estudios
Terapias ablativas alternativas
- La ablación por radiofrecuencia (ARF) es la terapia ablativa de primera línea basada en evidencia de nivel I.
- Según la guía del ACG, la crioterapia endoscópica puede considerarse como modalidad alternativa en pacientes que no responden a la ARF.
- Otras opciones incluyen la terapia fotodinámica, coagulación con plasma de argón, coagulación híbrida con plasma de argón y resección con EndoRotor.
Papel de la funduplicatura
Una revisión sistemática y metaanálisis demostró que la funduplicatura fue superior al tratamiento médico en cuanto a regresión histopatológica de la metaplasia/displasia de bajo grado (OR 4.38; IC 95% 2.28-8.42) y progresión a displasia/adenocarcinoma (OR 0.34; IC 95% 0.12-0.96). Sin embargo, la guía del ACG señala que los datos no demuestran de manera convincente que los pacientes tratados quirúrgicamente tengan menor riesgo de progresión neoplásica que los tratados médicamente, y no recomienda la funduplicatura de rutina como medida antineoplásica.La guía de la AGA de 2025 tampoco encontró un beneficio claro de la cirugía antirreflujo sobre el manejo médico para la progresión a adenocarcinoma esofágico.
La funduplicatura se reserva principalmente para pacientes con reflujo refractario al tratamiento médico que interfiere con la eficacia de la TEE.