Endoscopia en cáncer precoz
Limpieza de la mucosa
- Es importante la fotodocumentación para evaluar el grado de limpieza
- Existen varias escalas que permiten evaluar el grado de limpieza o preparación del estómago: escala de PEACE
- Es recomendable previo a la cromoendoscopia para mejorar la visualización de la mucosa
- Se recomienda el uso de antiespasmódicos antes de la endoscopia ( Butilbromuro de hioscina 10-20 mgs intramuscular o intravenoso; glucagón 1 mg endovenoso) y spray locales (aceite de pimienta o L-mentol 20 mL de 0.8% en spray). La hioscina se contraindica en pacientes con glaucoma, hiperplasia prostática, insuficiencia cardiaca e íleo paralítico. El glucagón se contraindica en pacientes con feocromocitoma y diabetes no controlada
- La mucosa gástrica puede no ser visualizada por algunos factores como la técnica endoscópica, moco en exceso, restos alimentarios, ingesta de alimentos, posición inadecuada, presencia de burbujas
- Se dispone de agentes mucolíticos son la Pronasa y N-acetilcisteína. La Pronasa es un agente mucolítico que se utiliza en Japón, es de gran utilidad en Cromoendoscopia y NBI. La Dimeticona reduce el tiempo del examen y la satisfacción endoscópica
Para el diagnóstico endoscópico de las lesiones gástricas incipientes, el paciente debe someterse a una preparación adecuada, que consiste en beber una solución con agua, un agente mucolítico y un detergente 30 min antes del procedimiento. El uso de esta preparación permite una mejor observación de la mucosa gástrica, identificar mejor las lesiones y guiar mejor la toma de biopsias así como la resección o disección de la mucosa
Endoscopia Superior
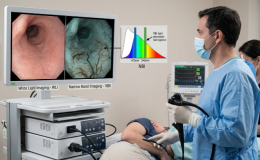
- La endoscopia convencional con luz blanca no puede detectar y caracterizar de manera precisa al cáncer precoz. Por tal motivo, es necesario el uso de cromoendoscopia (p. ej., índigo carmín) o de tecnologías de imagen endoscópica mejorada(p. ej., NBI)
- Es importante que el nivel de insuflación del estómago sea el adecuado para realizar un estudio exhaustivo de la mucosa gástrica
- Se recomienda que el tiempo mínimo de exploración de la mucosa gástrica debe ser de al menos 7 minutos
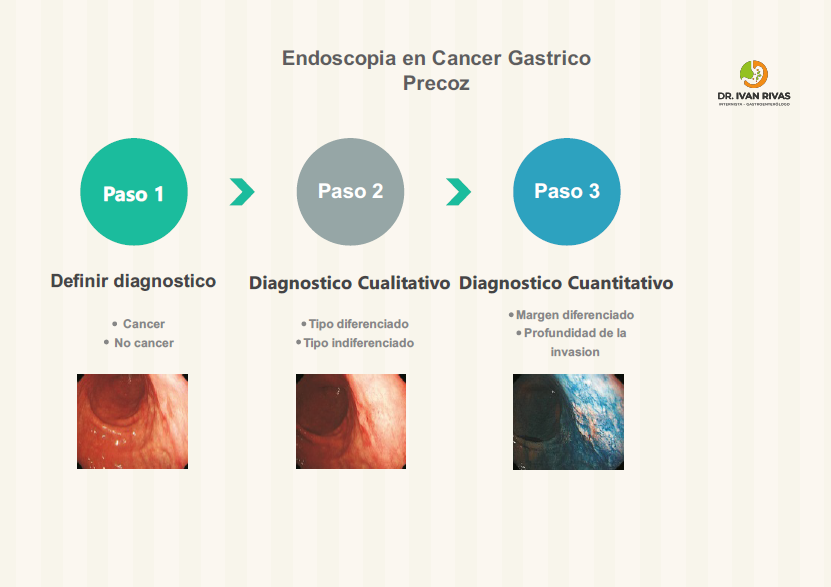
Existe cáncer?
Cual es la extensión de la lesión?
Cual es la profundidad de la lesión?
Si es posible predecir la histología de la lesión de acuerdo a los hallazgos endoscópicos?
A tener en cuenta
- Ante cualquier lesión sospechosa se recomienda describir tamaño y forma de la lesión (Clasificación de Paris), localización, patrón vascular y mucoso. Se debe documentar la lesión y tomar 2 biopsias dirigidas (Recomendación modificada)
- La luz blanca convencional no puede detectar ni caracterizar el cáncer precoz
- Se recomienda el uso de endoscopia de alta resolución con cromoendoscopia para la detección de cáncer precoz
- El uso de cromoendoscopia (Índigo Carmín) o técnicas endoscópicas de mejora de imagen (NBI) son las indicadas en este sentido
Tratamiento endoscópico
- La resección endoscópica es un tratamiento seguro,efectivo y mínimamente invasivo para el tratamiento de varias lesiones neoplásicas
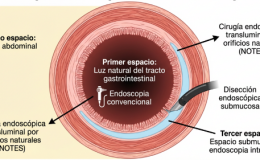
- La resección endoscópica incluye 2 tipos de procedimientos: la disección mucosal endoscópica (DME) y la resección mucosal endoscópica (RME)
- La resección endoscópica suele ser muy efectiva cuando se realiza en manos expertas y con las indicaciones adecuadas
La elección del tipo de procedimiento (RME o DME) depende de ciertos factores: resultados de la biopsia, tamaño de la lesión, profundidad de la invasión, presencia de ulceración
Diagnóstico diferencial de lesiones precoces gástricas
Ante la sospecha de CGP se deben estudiar tres características:
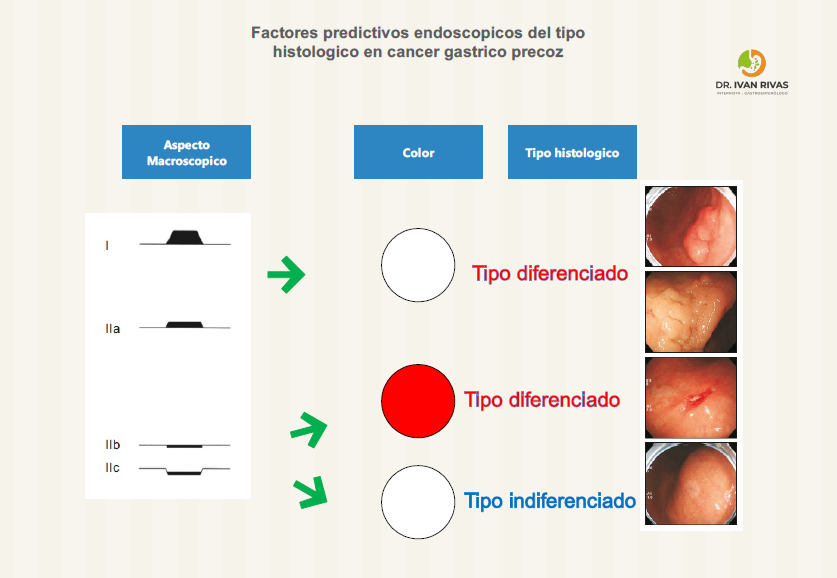
- Color de la lesión
- Morfología de la lesión
- Línea de demarcación
Lesiones elevadas
- Son las más fáciles de detectar
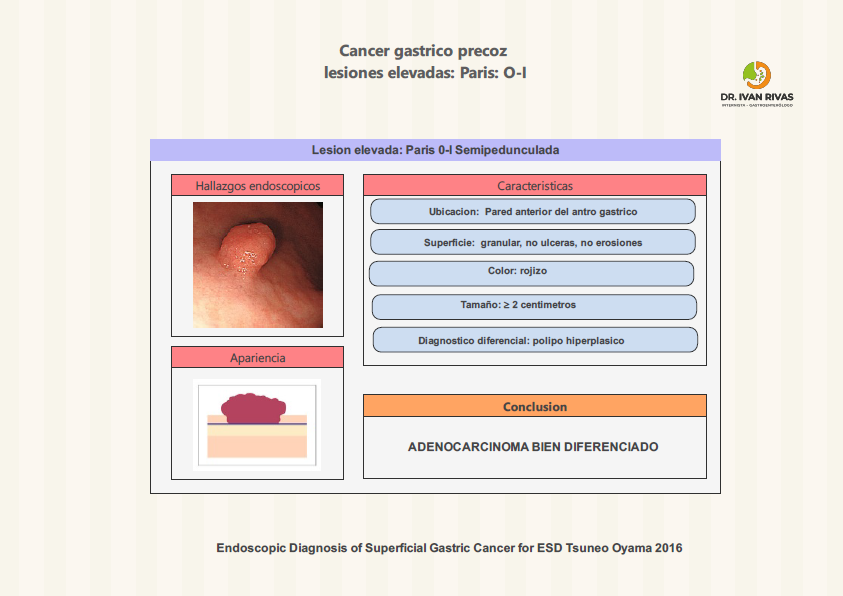
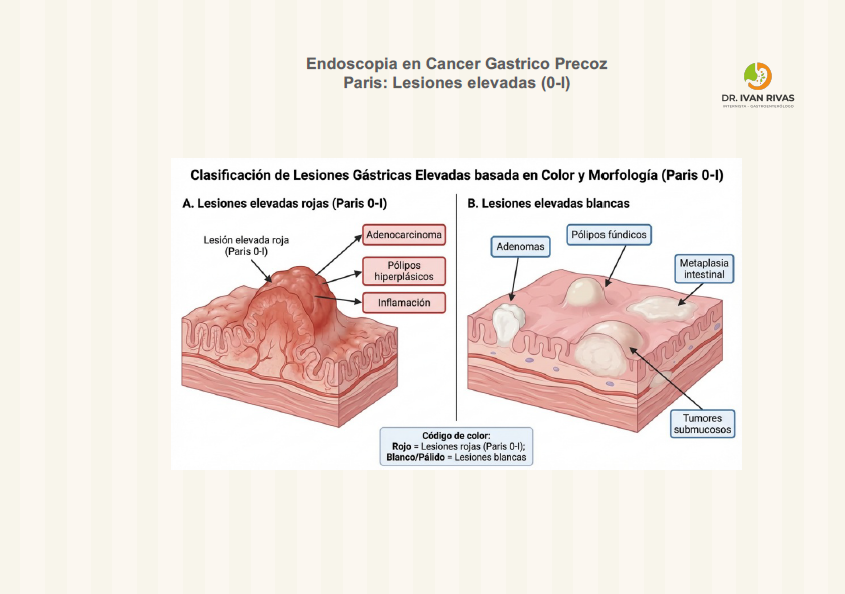
- El diagnóstico diferencial es con los adenocarcinomas bien diferenciados y adenomas tubulares, se deben descartar también con pólipos hiperplásicos, pólipos fúndicos glandulares o metaplasia intestinal
- Se debe observar el color, forma, demarcación y patrones superficiales
- Los adenocarcinomas bien diferenciados, pólipos hiperplásicos o inflamación son lesiones protuberantes rojas
- Los adenomas, pólipos de glándulas fúndicas, metaplasia intestinal o tumores submucosos son lesiones protuberantes blancas
- Las neoplasias superficiales como el adenocarcinoma gástrico o el adenoma tubular tienen bordes bien delimitados
- Los cambios inflamatorios y las neoplasias de origen no epitelial como la gastritis, linfoma maligno no tienen bordes definidos
- Hay que observar si la superficie es lisa, suave o nodular. Observar la presencia de áreas de depresión central
Lesiones deprimidas
- Las lesiones deprimidas más frecuentes son las erosiones y la atrofia focal
- Diagnóstico diferencial: adenocarcinomas bien diferenciados, adenocarcinomas mal diferenciados y linfomas tipo Malt
- Los adenocarcinomas son lesiones irregulares bien diferenciadas con bordes bien definidos
- Lesiones deprimidas rojas: los adenocarcinomas bien diferenciados tienen estructuras glandulares con proliferación de vasos por lo que su color es rojo.
- Lesiones deprimidas blanquecinas: adenocarcinomas mal diferenciados
Procedimientos endoscópicos utilizados en cáncer precoz
La RME es ideal para lesiones pequeñas, bien definidas. La DME se recomienda para lesiones grandes (permite resección en bloque). Otras técnicas ablativas (Radiofrecuencia o Crioterapia) se utiliza para lesiones planas con cambios displásicos en el esofago
Resección mucosal endoscópica (RME)
- Utiliza técnicas básicas utilizando un asa para resecar la mucosa con o sin la asistencia de de ligas y capuchones
- Los especímenes pueden ser removidos en bloque generalmente son menores a 2 cms (20 mm) mientras las lesiones más grandes requieren resección en fragmentos. La limitación en el tamaño no permite la resección de lesiones más grandes ya que no se obtienen márgenes de resección adecuados
Disección mucosal endoscópica (DME)
- Permite la resección en bloque de lesiones de mayor tamaño (disminuye la recurrencia)
- Es un procedimiento complejo que incluye varias etapas
- Se considera el tratamiento de elección para la mayoría de lesiones precoces
Determinar la presencia de enfermedad invasiva representa un reto ya que la biopsia mucosa generalmente no incluye fragmentos representativos de la submucosa
La decisión de llevar a cabo RME o DME depende de factores relacionados con la lesión y con el paciente. Se considera que las lesiones pequeñas (premalignas o malignas) sin componente invasivo pueden ser manejadas con RME. El manejo de lesiones de mayor tamaño y con invasión submucosa es menos claro.
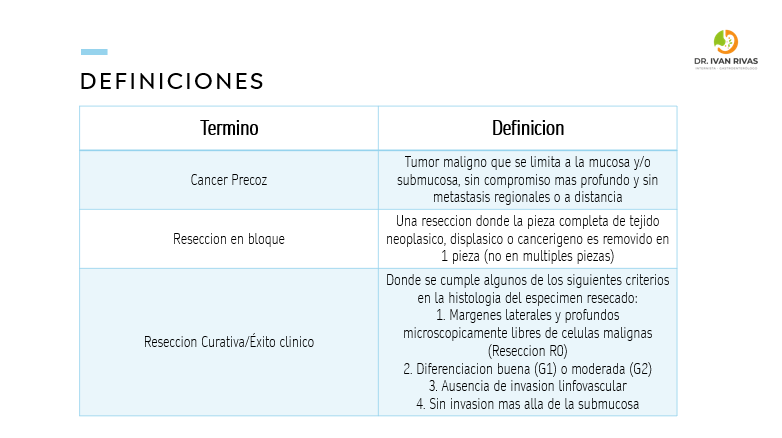
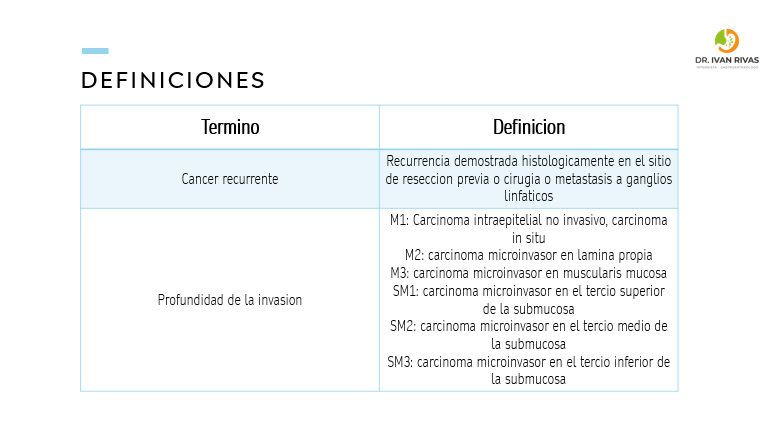
Definiciones
Cancer precoz de esofago
- La neoplasia de células escamosas o epidermoides incluye varios tipos de neoplasia: displasia de bajo grado, displasia de alto grado, carcinoma in situ, carcinoma invasor
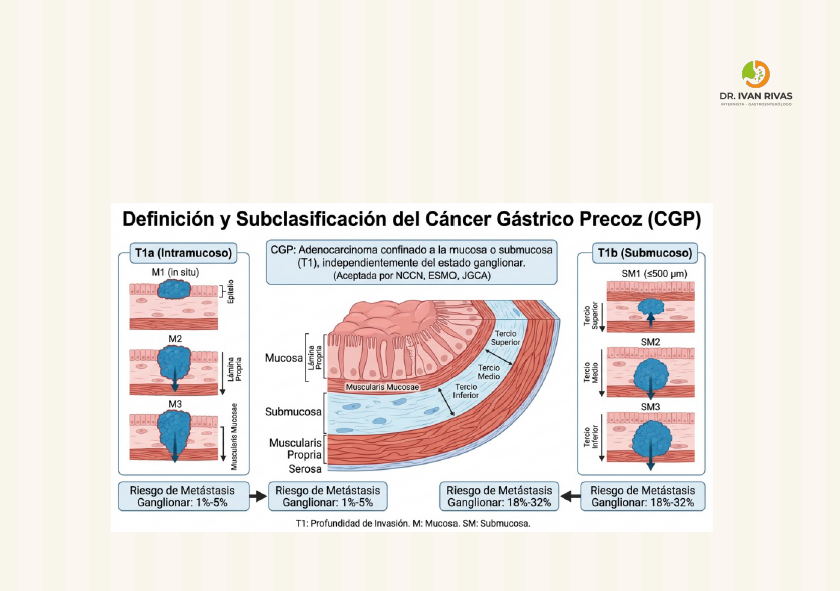
- La profundidad de la invasión mucosa para carcinomas invasivos se subdivide en: M1 (Carcinoma in situ), M2 (carcinoma microinvasor en la lámina propia) y M3 (invasión a la muscularis mucosa)
- La profundidad de la invasión a la submucosa se clasifica en tercio superior (SM1), tercio medio (SM2) y tercio inferior (SM3)
- La profundidad de la invasión no puede ser determinada en los especímenes obtenidos de la DME
- En el esofago la profundidad de la invasión SM1 es mayor o igual a 200 um
- Para el esofago de Barrett se considera displasia de bajo grado, displasia de alto grado y carcinoma. El carcinoma invasor que se extiende a la submucosa se clasifica de SM1-SM3
Clasificacion del cancer de esofago
El cancer precoz del esofago se clasifica y categoriza utilizando varios sistemas de clasificación siendo los más utilizados el del Comité Americano sobre el cancer (AJCC) y la Unión Internacional para el control del cáncer o TNM. Esto incluye la profundidad de la lesión (T), compromiso ganglionar (N) y la presencia de metástasis a distancia (M)
Estadiaje TNM:
- Tis: displasia de alto grado o carcinoma in situ, se define como la lesión confinada al epitelio sobre la membrana basal
- T1: la lesión invade la lámina propia, muscularis mucosa (T1a) o submucosa (T1b). La diferencia entre T1a y T1b tiene significancia clínica debido a que las lesiones T1b (invasión submucosa) tiene mayor riesgo de metástasis ganglionar
- Ganglios linfáticos (N): N0(Ninguno); N1(1-2); N2 (3-6); N3(mayor o igual a 7)
- Metástasis (M): M0 (sin metástasis a distancia); M1(metástasis a distancia). Se requiere M0 para enfermedad precoz
Subtipo histológico y grado:
- La AJJC/UICC separa el carcinoma de células escamosas del adenocarcinoma para el estadiaje, reflejando diferencias entre su biología y pronóstico
- Se incorpora el grado del tumor: G1 (bien diferenciado); G2 (moderadamente diferenciado); G3 (pobremente diferenciado). El grado tiene influencia en el estadiaje, especialmente para lesiones T1
Clasificación WHO:
- La Organización Mundial de la Salud (WHO) clasifica los tumores epiteliales como benignos, displásicos (bajo y alto grado) o malignos ( adenocarcinoma, carcinoma de células escamosas y otros tipos menos frecuentes)
- La displasia se divide en Barrett y displasia escamosa, de bajo y de alto grado
Criterios patológicos adicionales:
- Para invasión submucosa, la profundidad de la lesión a veces es subclasificado (SM1 menor o igual a 500 micromicras) para guiar la terapia endoscópica particularmente para el adenocarcinoma
Hallazgos endoscopicos en cancer precoz de esofago
- Tanto el cáncer epidermoide como el adenocarcinoma producen cambios muy sutiles a nivel de la mucosa esofágica
- Cáncer escamoso o epidermoide: la luz blanca demuestra lesiones planas, elevadas o deprimidas. Se pueden apreciar áreas de decoloración, erosiones o irregularidad de la superficie mucosa. Las lesiones que se limitan al epitelio o a la lámina propia (T1a) son generalmente planas sin elevación o depresión, mientras que aquellas que comprometen la muscularis mucosa o la submucosa superficial (T1b-SM1) pueden mostrar áreas elevadas o deprimidas menores a 1mm
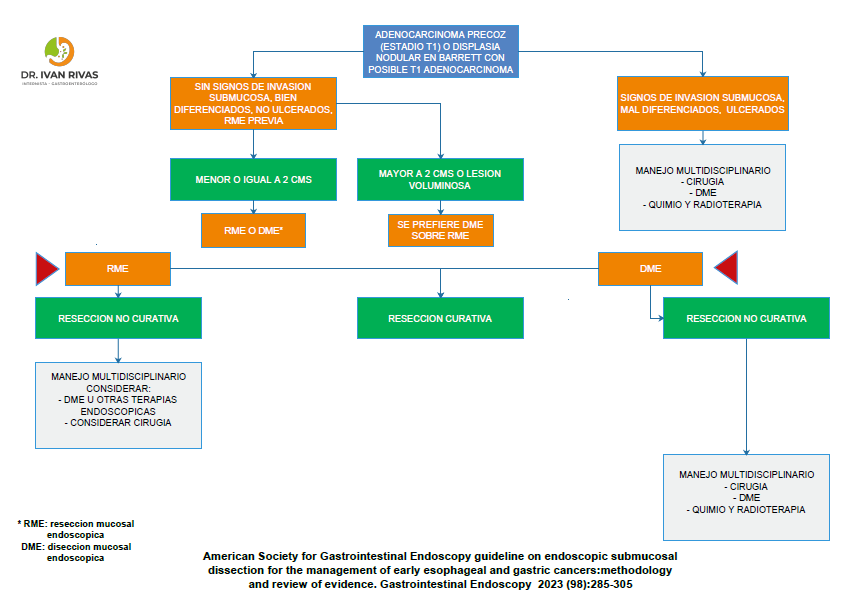
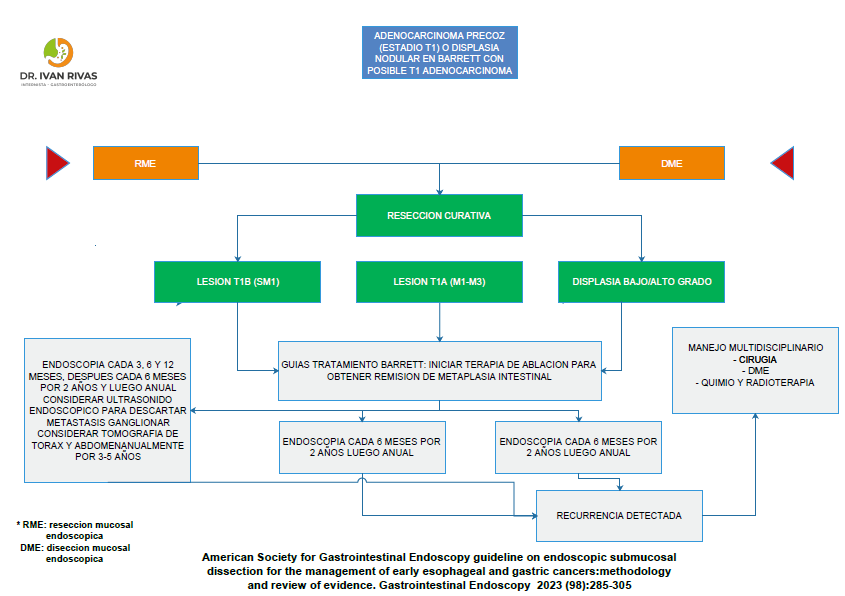
Tratamiento endoscópico
Indicaciones mucosectomía en Cancer de Esofago
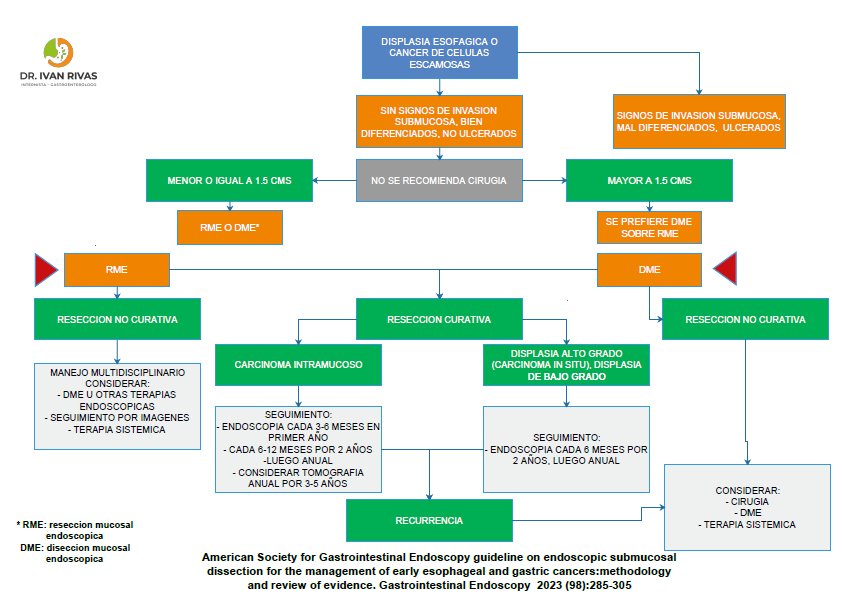
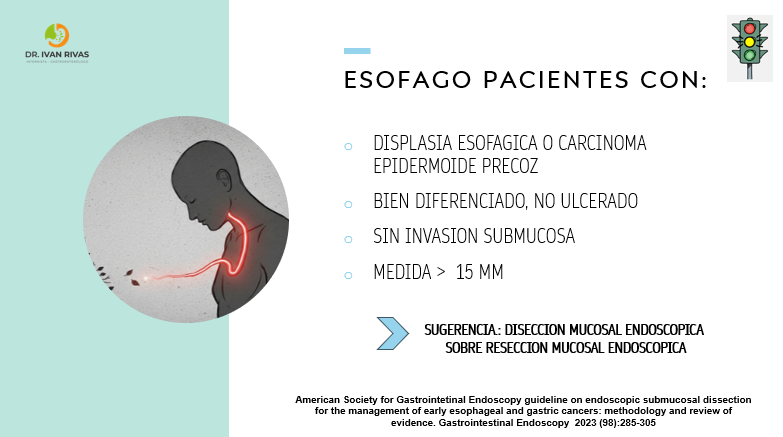
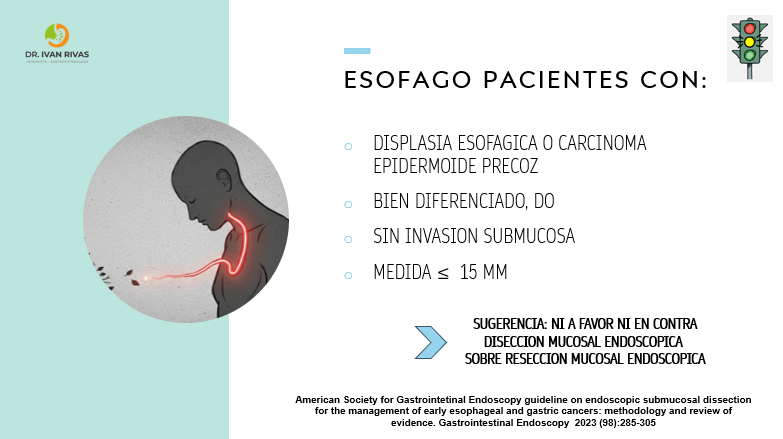
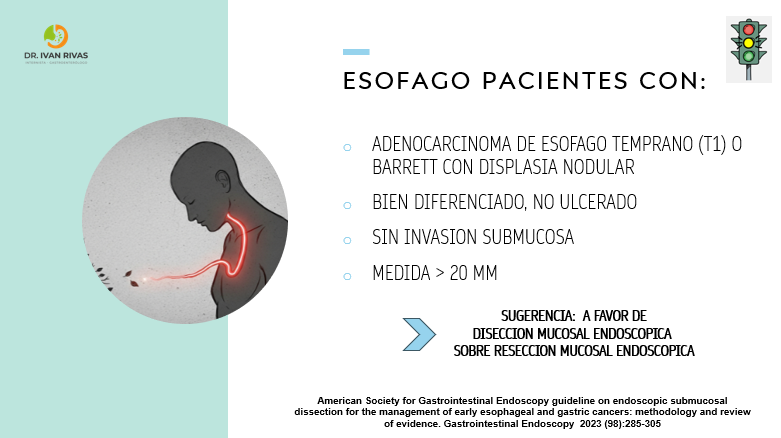
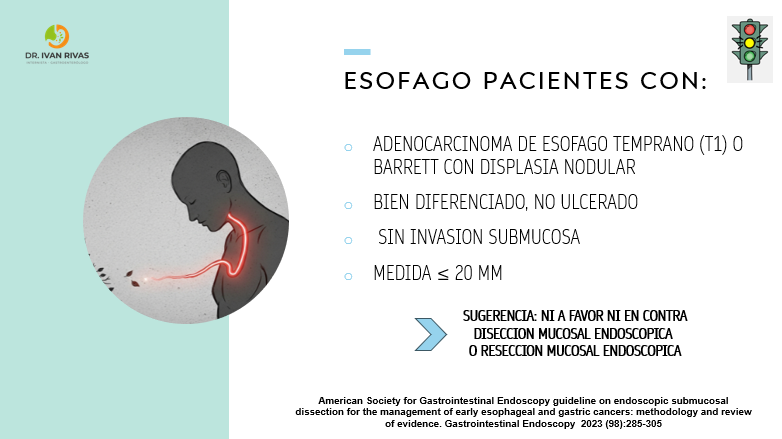
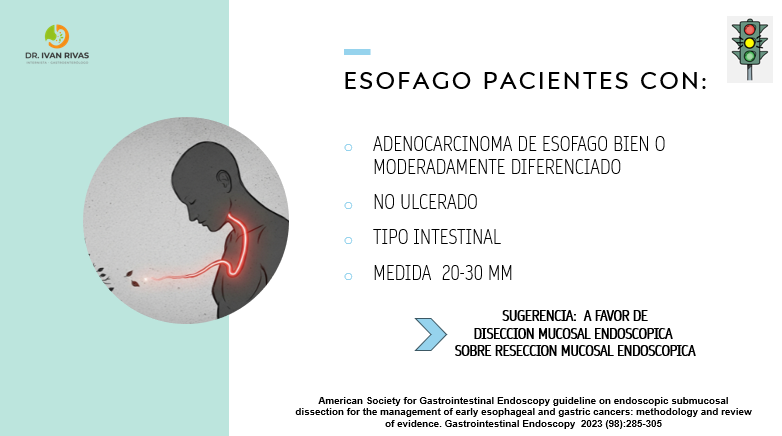
Que procedimiento debe realizarse en pacientes con displasia o carcinoma esofagico precoz bien diferenciado, no ulcerado?
- Lesión mayor de 15 mm: se sugiere DME sobre RME
- Lesión menor o igual a 15 mm: puede ser DME o RME
Cáncer precoz de estómago
- El cáncer gástrico precoz (CGP) es aquel que se encuentra limitado a la mucosa y submucosa, independientemente de la presencia de metástasis a ganglios linfáticos
- El concepto original de CGP se estableció en Japón en 1962 y se definia como una neoplasia gástrica que puede ser tratada de forma exitosa con cirugía. El estadiaje TNM del CGP es T1 y cualquier N1. Estos tumores tienen un mejor pronóstico comparado con otros estadios y una sobrevida mayor al 90%
- Los factores de riesgo para metástasis ganglionar con la edad > de 60 años, tipo macroscópico deprimido, ulceración, tamaño > 2-3 cms, tipo histológico indiferenciado, invasión de nódulos linfáticos, invasión submucosa profunda (>500 um) y fenotipo mucinoso
- La incidencia de CGP se ubica entre el 15-57% de los casos de adenocarcinoma gástrico, dependiendo del área geográfica y de los programas de seguimiento.
Principios Endoscópicos en la evaluación de pacientes con sospecha de cáncer gástrico precoz
Recomendaciones previas y durante la endoscopia
Las guías de calidad de la ACG/AGA y la ASGE recomiendan:
- Ayuno preprocedimiento: no ingerir líquidos claros por al menos 2 horas, leche por 6 horas, comida ligera por 6 horas, y alimentos grasos o fritos por 8 horas antes de la sedación. Pacientes con gastroparesia o acalasia pueden requerir un período de ayuno más prolongado
- Evaluación preprocedimiento: historia clínica dirigida que incluya condiciones que afecten la seguridad del procedimiento, antecedentes de reacciones adversas a sedación/anestesia, alergias medicamentosas, medicamentos actuales e interacciones potenciales, y uso de tabaco, alcohol o sustancias
- Examen físico dirigido: al menos examen abdominal basal, y auscultación cardiopulmonar si hay preocupación por el estado cardiorrespiratorio
- Manejo de anticoagulantes y antiagregantes: ajustar según las guías vigentes de manejo periprocedimiento
- Consideración de agonistas del receptor GLP-1: en pacientes que toman estos fármacos u otros que retrasen el vaciamiento gástrico, se deben seguir las políticas institucionales actualizadas para minimizar el riesgo de aspiración
- Consentimiento informado: el paciente debe ser informado de que, si se diagnostica cáncer, podría requerirse tratamiento adicional incluyendo cirugía, dependiendo del grado y estadio
La premedicación con soluciones de limpieza mucosa antes de la endoscopia superior mejora significativamente la visibilidad gástrica, lo cual es particularmente relevante en la evaluación de cáncer gástrico precoz. La AGA recomienda el uso de agentes de limpieza mucosa como parte de la endoscopia de alta calidad, y la ESGE incluye la documentación de un puntaje de visibilidad mucosa como indicador de calidad.
A continuación se detallan los agentes disponibles, las combinaciones más estudiadas y el momento óptimo de administración:
Agentes de limpieza mucosa disponibles:
- Agentes antiespumantes (simeticona/dimeticona): Reducen las burbujas intraluminales al disminuir la tensión superficial. La simeticona (100-200 mg) mejora la visualización mucosa en la mayoría de los estudios, particularmente en esófago y duodeno
- Mucolíticos (N-acetilcisteína, NAC): Disuelven el moco adherido a la mucosa gástrica. La NAC (500-1000 mg) combinada con simeticona mejora significativamente la visibilidad gástrica comparada con simeticona sola o agua
- Enzimas proteolíticas (pronasa): Degradan las proteínas del moco gástrico. La pronasa (20,000 U) es ampliamente utilizada en Japón y Corea del Sur como parte del protocolo estándar de detección de cáncer gástrico precoz. Mejora la visibilidad especialmente en el cuerpo gástrico proximal y el fondo

Características endoscópicas
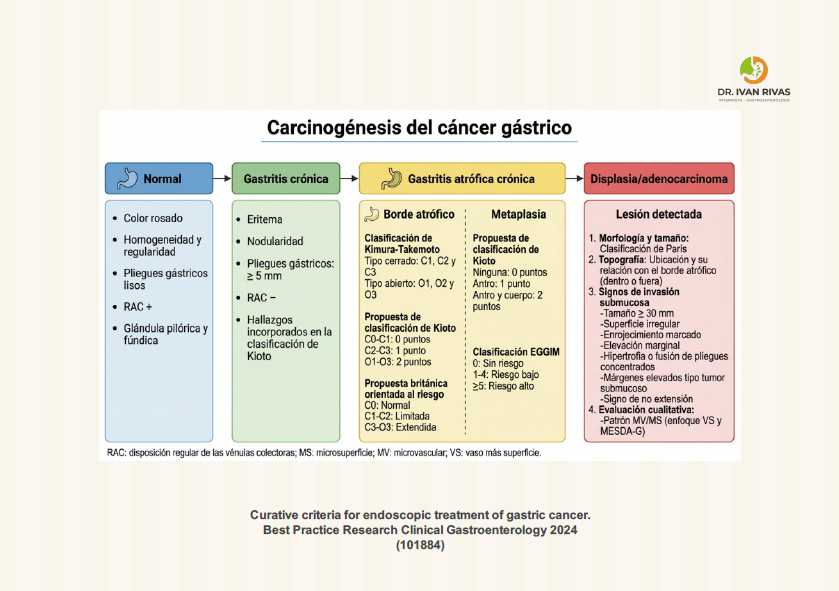
La carcinogénesis del cáncer gástrico es un proceso multifactorial y multietapa que involucra la interacción entre factores infecciosos (principalmente Helicobacter pylori), ambientales, genéticos y epigenéticos, culminando en la transformación maligna del epitelio gástrico
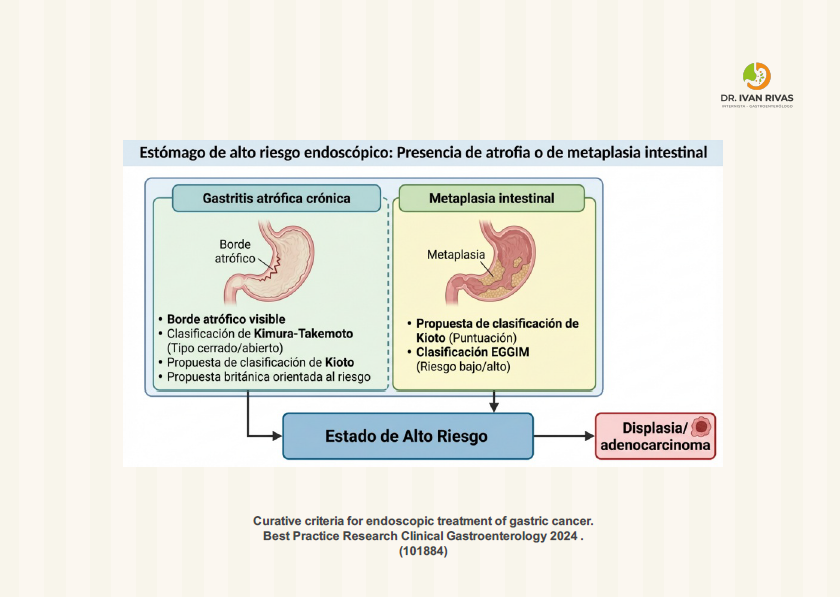
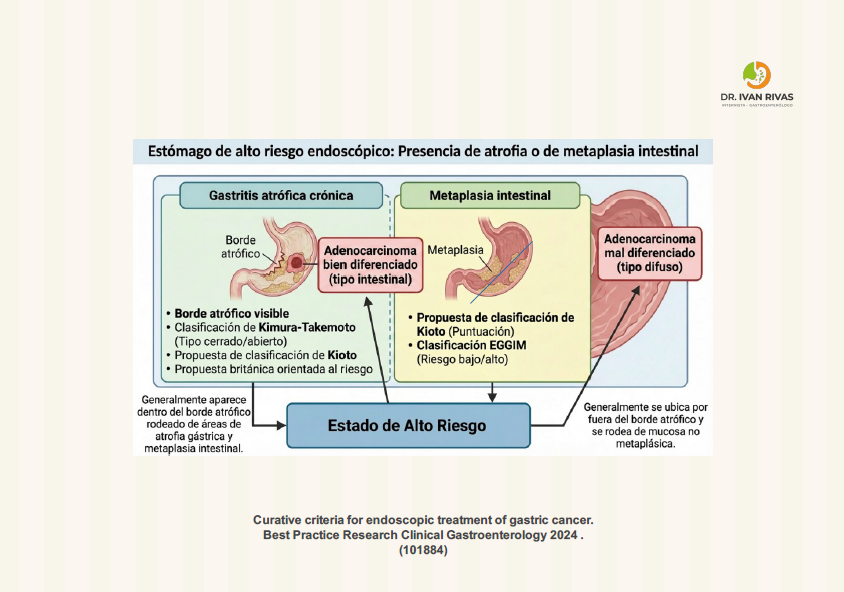
Clasificacion de Kimura Takemoto
La American Gastroenterological Association reconoce la clasificación de Kimura-Takemoto como un sistema endoscópico válido para evaluar la extensión de la atrofia gástrica basándose en la identificación del borde atrófico. Este sistema, propuesto en 1969, categoriza la atrofia gástrica en tipo cerrado (C) o tipo abierto (O), cada uno con grados según la extensión del borde atrófico. Utilidad clínica para estratificación de riesgo de cáncer gástrico: Múltiples estudios han demostrado consistentemente que la atrofia severa o extensa (tipos O2-O3) se asocia con un riesgo acumulativo significativamente mayor de cáncer gástrico en comparación con la atrofia leve (tipos C1-C2).Estos hallazgos son concordantes con los sistemas de estadificación histológica OLGA/OLGIM.
Aplicación en diferentes etiologías: La clasificación es particularmente útil para evaluar la gastritis atrófica asociada a Helicobacter pylori (HpAG), donde la atrofia típicamente se inicia en el antro gástrico y se expande proximalmente, pudiendo involucrar todo el estómago en casos severos. En contraste, en la gastritis autoinmune (AIG), la atrofia afecta principalmente el cuerpo y fondo gástrico con preservación característica del antro.
Técnica endoscópica: Para maximizar el rendimiento diagnóstico, los endoscopistas deben realizar un examen de alta calidad con visualización óptima de la mucosa, incluyendo insuflación adecuada de aire, limpieza mucosa, y examen sistemático de toda la mucosa gástrica. Las características endoscópicas típicas de la atrofia incluyen apariencia pálida de la mucosa, aumento de la visibilidad de los vasos submucosos debido al adelgazamiento de la mucosa gástrica, y pérdida de los pliegues gástricos.
Metaplasia Intestinal
Los hallazgos endoscópicos característicos de la metaplasia intestinal gástrica incluyen apariencia nodular con patrones mucosos en crestas o tubulovellosos, el signo de “cresta azul claro” (light blue crest), y los campos opacos blancos (white opaque substance).
Estos hallazgos son más fácilmente identificables con endoscopia de alta definición con luz blanca (HD-WLE) y se mejoran significativamente con tecnologías de imagen mejorada como la imagen de banda estrecha (NBI).
Hallazgos con endoscopia de luz blanca de alta definición:
Las áreas con metaplasia intestinal típicamente aparecen con las siguientes características:
- Apariencia nodular
- Patrones mucosos en crestas o tubulovellosos
- Mucosa blanquecina
- Superficie mucosa rugosa
- Apariencia vellosa
Hallazgos con imagen de banda estrecha (NBI):
El NBI mejora significativamente la detección de metaplasia intestinal, con sensibilidad y especificidad de 87% y 97% respectivamente. Los hallazgos característicos incluyen:
- Signo de “cresta azul claro” (light blue crest – LBC): Líneas finas azul-blancas en las crestas de la superficie epitelial, con sensibilidad y especificidad de aproximadamente 90%
- Campos opacos blancos (white opaque substance): Resultado de gotas lipídicas microscópicas que se acumulan en la mucosa, con especificidad muy alta (100%) pero sensibilidad limitada (50%)
- Patrón B en la clasificación NBI simplificada: Mucosa tubulovellosa asociada con metaplasia intestinal (precisión 84%)
Los estudios multicéntricos prospectivos demuestran que el NBI sin magnificación detecta metaplasia intestinal en 32% más de pacientes comparado con luz blanca sola (70% vs 38%). La sensibilidad y especificidad del NBI y LCI sin magnificación exceden 85-90% para la detección de metaplasia intestinal gástrica.
La American Gastroenterological Association recomienda que los endoscopistas reconozcan las características visuales típicas de la metaplasia intestinal, ya que estos hallazgos frecuentemente no se diagnostican cuando los endoscopistas no están familiarizados con ellos. Cuando se sospecha metaplasia intestinal, se deben obtener biopsias según un protocolo sistemático (como el Sistema Sydney actualizado) con un mínimo de 5 biopsias totales, con muestras del antro/incisura y cuerpo colocadas en frascos separados.
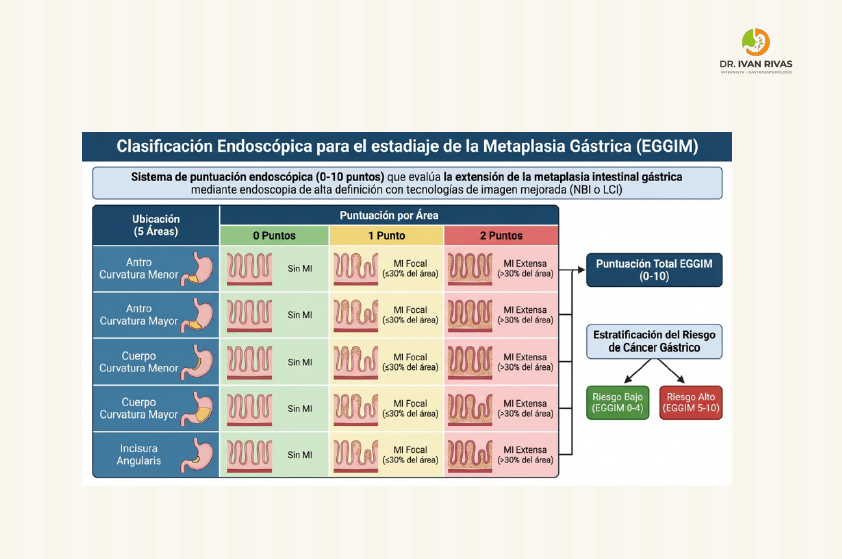
Clasificación EGGIM para metaplasia gástrica
La clasificación EGGIM (Endoscopic Grading of Gastric Intestinal Metaplasia) es un sistema de puntuación endoscópica que evalúa la extensión de la metaplasia intestinal gástrica mediante endoscopia de alta definición con técnicas de imagen mejorada (narrow-band imaging o linked color imaging), permitiendo la estratificación del riesgo de cáncer gástrico sin necesidad de biopsias múltiples.
El sistema EGGIM asigna una puntuación de 0 a 10 basada en la evaluación endoscópica de cinco áreas anatómicas del estómago:
- Curvatura menor del antro
- Curvatura mayor del antro
- Incisura angularis
- Curvatura menor del cuerpo gástrico
- Curvatura mayor del cuerpo gástrico
Para cada área, se asigna una puntuación según la extensión de la metaplasia intestinal visible endoscópicamente:
- 0 puntos: Sin metaplasia intestinal
- 1 punto: Metaplasia intestinal focal (≤30% del área)
- 2 puntos: Metaplasia intestinal extensa (>30% del área)
La suma de las puntuaciones de las cinco áreas genera el puntaje EGGIM total (0-10)
Estratificación del riesgo de cáncer gástrico
El punto de corte crítico para la estratificación del riesgo es EGGIM ≥5, que identifica pacientes con alto riesgo de neoplasia gástrica temprana:
EGGIM 0-4 (bajo riesgo):
- Correlaciona con OLGIM (Operative Link on Gastric Intestinal Metaplasia) estadios 0-II
- Riesgo bajo de progresión a cáncer gástrico
EGGIM 5-10 (alto riesgo):
- Correlaciona con OLGIM estadios III-IV (sensibilidad 89-92%, especificidad 90-95%, AUC 0.96-0.97)
Ventajas clínicas del EGGIM:
- Reducción de biopsias: Permite identificar pacientes de alto riesgo mediante evaluación endoscópica dirigida, reduciendo la necesidad de biopsias aleatorias múltiples según el sistema Sydney
- Correlación con histología: Muestra excelente concordancia con el sistema histológico OLGIM, considerado el estándar de oro
- Aplicabilidad práctica: Puede realizarse durante la endoscopia de rutina con técnicas de imagen mejorada disponibles en la mayoría de centros (NBI, LCI)
- Guía de vigilancia: Los pacientes con EGGIM ≥5 se benefician de vigilancia endoscópica cada 2-3 años, mientras que aquellos con EGGIM <5 pueden no requerir vigilancia intensiva
Limitaciones y consideraciones:
- Dependencia del operador: La precisión diagnóstica depende de la experiencia del endoscopista y del entrenamiento en técnicas de imagen mejorada
- Validación geográfica: La mayoría de estudios provienen de Europa y Asia; la validación en poblaciones occidentales, especialmente en Estados Unidos, es limitada
- Complementariedad con histología: Aunque EGGIM puede reducir biopsias, las guías actuales de la AGA recomiendan que la estratificación histológica (subtipo de metaplasia, severidad, extensión) siga siendo documentada para decisiones clínicas óptimas
- Inteligencia artificial: Estudios recientes muestran que sistemas de IA pueden estimar EGGIM con precisión del 88% para decisiones de vigilancia (EGGIM ≥5), con tasa de falsos negativos del 0%, lo que podría mejorar la reproducibilidad
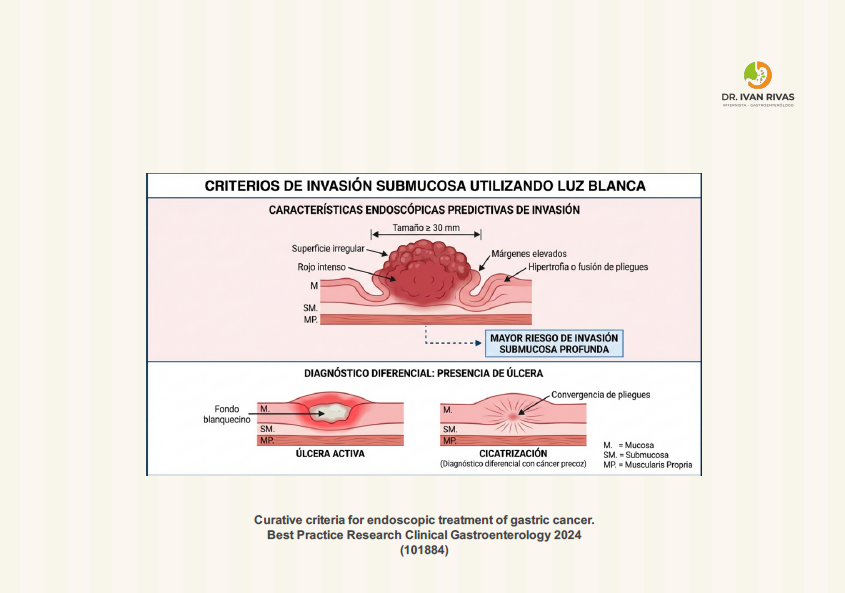
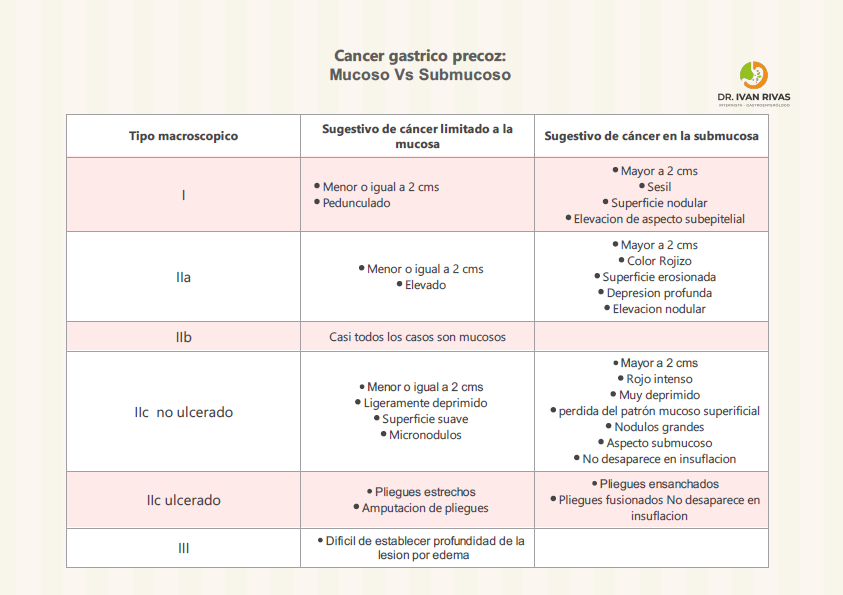
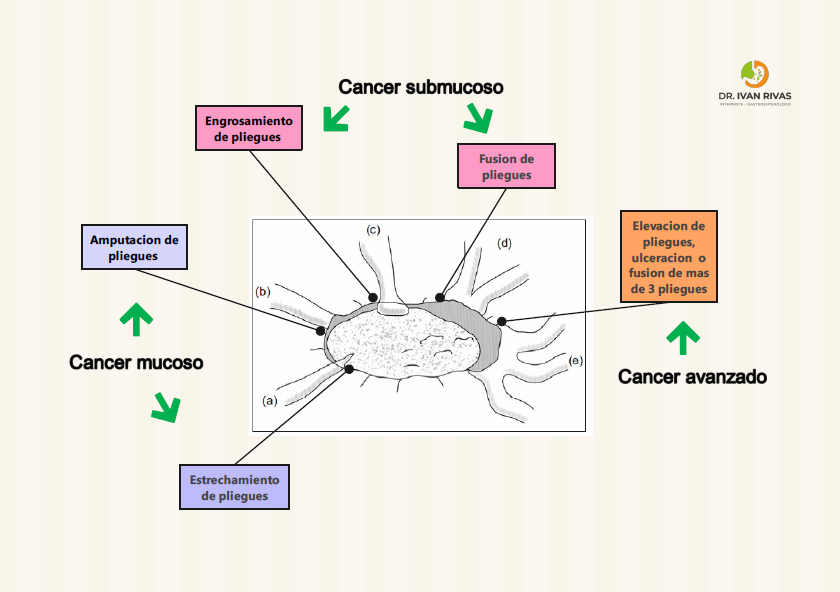
Criterios de invasión submucosa del cáncer gástrico precoz
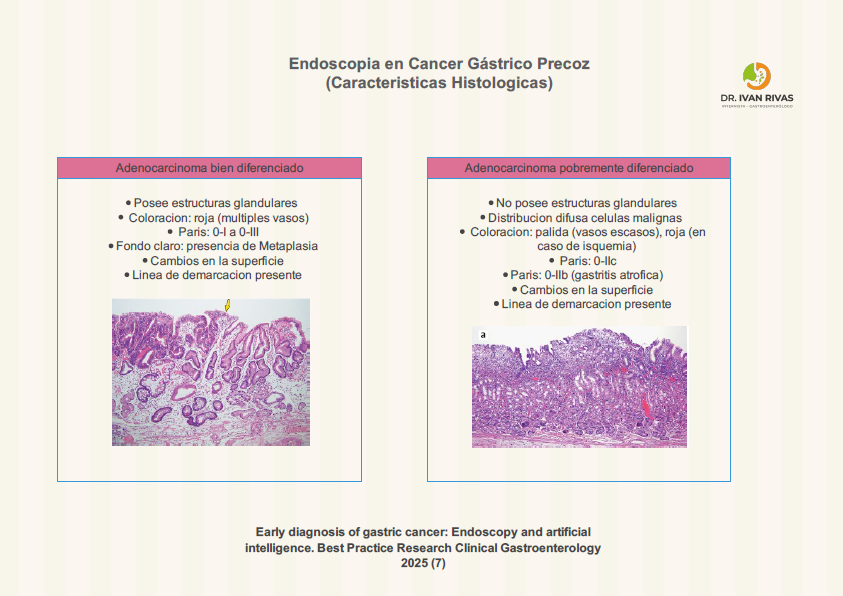
Características Histológicas
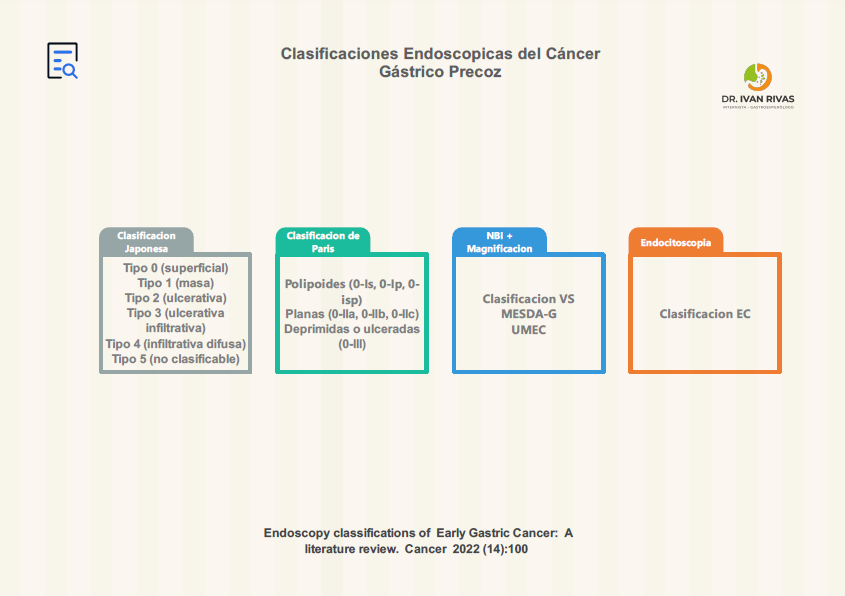
Clasificación Endoscópica
- Se han desarrollado algunas clasificaciones morfológicas que permiten predecir invasibilidad como la clasificación de Paris, la clasificación de Kudo y otras basadas en Narrow Banding Imaging
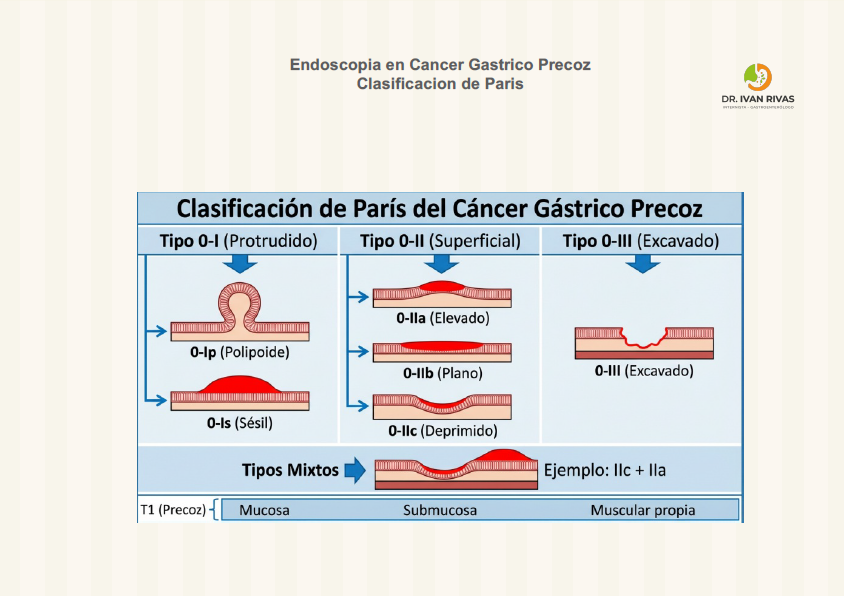
Clasificación de París
La Clasificación de París para lesiones neoplásicas superficiales del tracto digestivo, incluido el cáncer gástrico precoz, surge como una respuesta a la necesidad de estandarizar la descripción endoscópica de estas lesiones y mejorar la correlación entre la morfología endoscópica y el riesgo de invasión submucosa. Su desarrollo se basa en la experiencia japonesa, donde se reconoció que la morfología superficial (tipo 0) tenía implicancias pronósticas y terapéuticas relevantes. En 2002, un taller internacional en París revisó la clasificación japonesa y propuso una adaptación internacional, que fue posteriormente refinada en Osaka en 2003, estableciendo subtipos morfológicos (protruidas, planas, deprimidas y excavadas) y su relación con el riesgo de invasión y metástasis ganglionar.
La “clasificación de París” para el cáncer gástrico precoz es un sistema endoscópico ampliamente utilizado para categorizar las lesiones superficiales del tracto digestivo, incluyendo el estómago, según su morfología macroscópica. Esta clasificación distingue entre lesiones polipoides y no polipoides, lo que es fundamental para la evaluación endoscópica y la decisión terapéutica en el cáncer gástrico precoz.
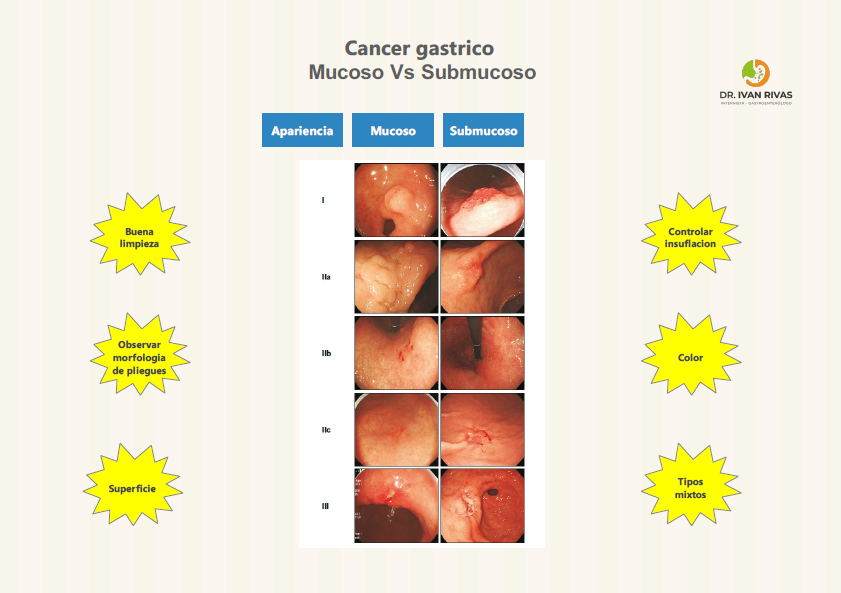
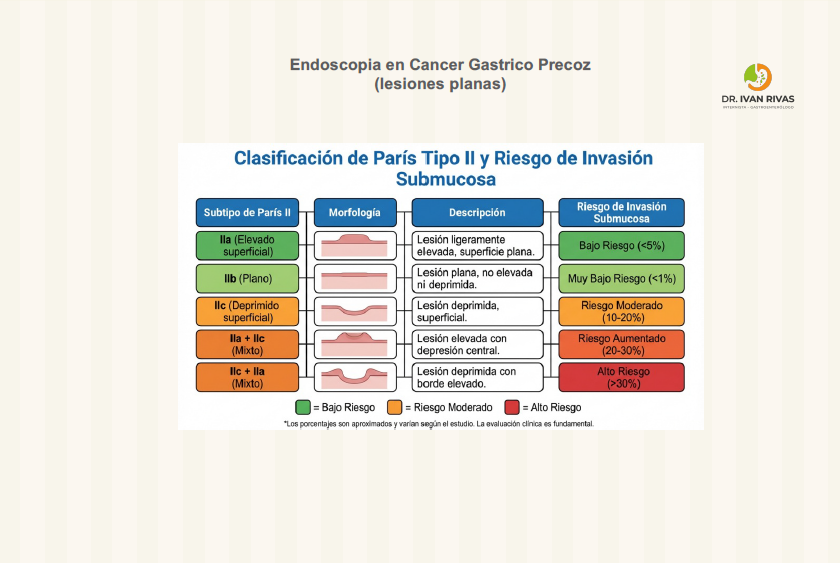
La clasificación de París divide las lesiones en:
- Tipo 0-I: Lesiones polipoides (protruidas)
- Tipo 0-II: Lesiones no polipoides, subdivididas en:
- 0-IIa: Elevadas.
- 0-IIb: Planas.
- 0-IIc: Deprimidas.
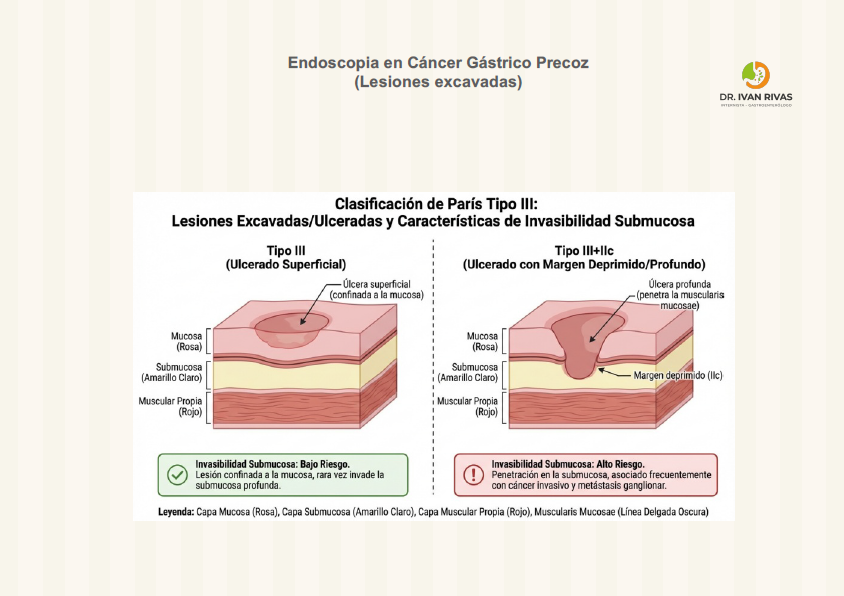
- Tipo 0-III: Lesiones excavadas (ulceradas).
En la práctica clínica, la mayoría de los cánceres gástricos precoces corresponden a los tipos 0-IIc y combinaciones como 0-IIc+IIa, que tienen implicaciones pronósticas y terapéuticas, ya que las lesiones deprimidas suelen asociarse a mayor riesgo de invasión submucosa y, por tanto, mayor riesgo de metástasis ganglionar
La Clasificación de París permite una evaluación sistemática y reproducible de las lesiones superficiales del estómago, facilitando la estimación endoscópica de la profundidad de invasión y, por ende, la selección del tratamiento más adecuado (resección endoscópica o quirúrgica).
Clasificación de Paris: lesiones elevadas
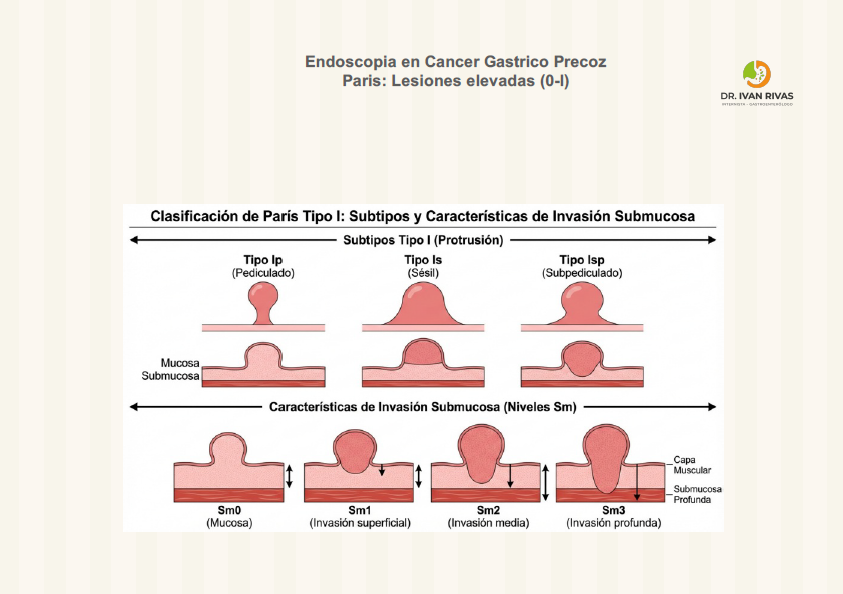
- Según la Clasificación de París, las lesiones elevadas del tracto gastrointestinal se dividen en dos grandes grupos según su morfología y relación con la mucosa circundante: polipoides (protruidas) y no polipoides (superficialmente elevadas). Las polipoides corresponden al tipo 0-I, que se subdivide en pedunculadas (0-Ip), cuando presentan un tallo, y sésiles (0-Is), cuando la base es amplia y está en contacto directo con la mucosa
- Por otro lado, las lesiones elevadas no polipoides se clasifican como tipo 0-IIa, que son aquellas que presentan una elevación discreta sobre la mucosa, sin formar un pólipo definido ni tener un tallo, y cuya protrusión es menor a 2.5 mm
- Esta distinción es relevante porque las lesiones tipo 0-IIa suelen tener un menor riesgo de invasión submucosa comparado con las lesiones deprimidas (0-IIc), y la evaluación precisa de la morfología es fundamental para la toma de decisiones terapéuticas
En resumen, la Clasificación de París categoriza las lesiones elevadas en:
- Tipo 0-Ip: polipoide pedunculada
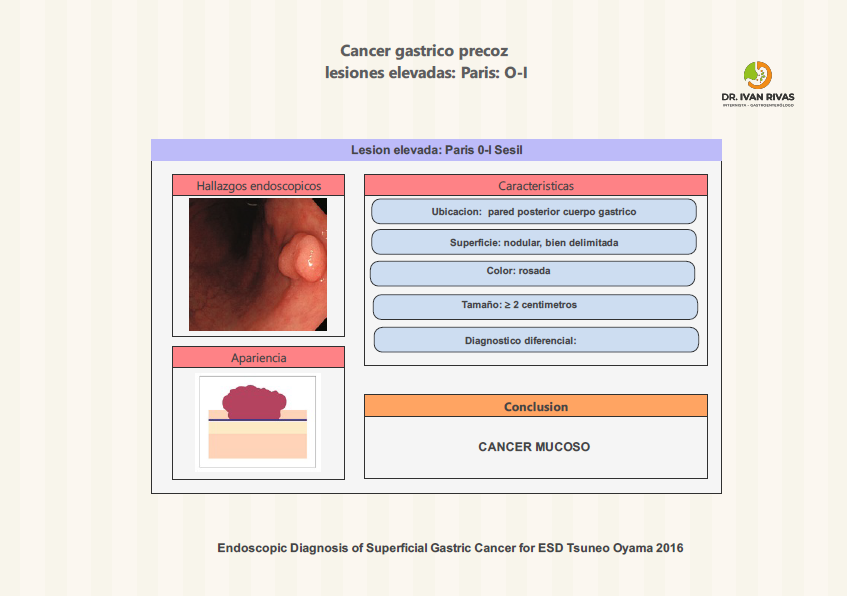
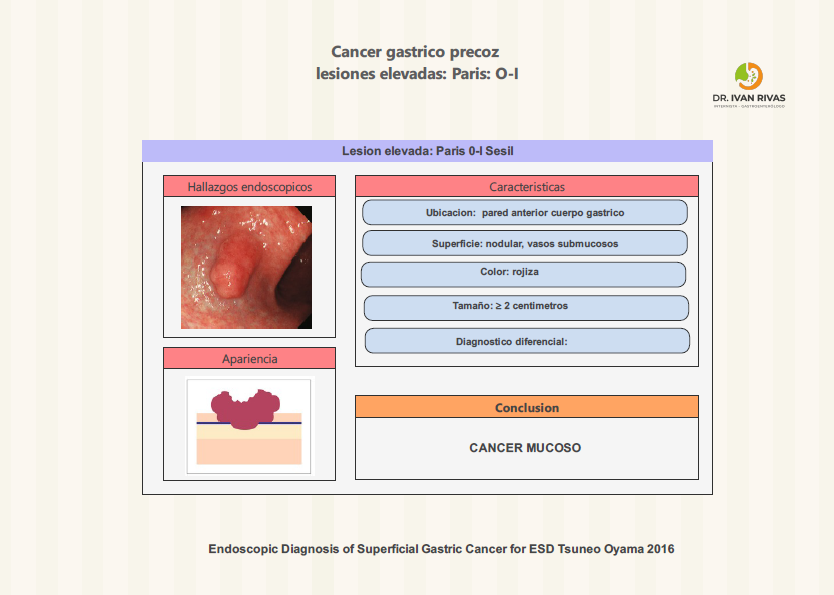
- Tipo 0-Is: polipoide sésil
- Tipo 0-IIa: superficialmente elevada no polipoide
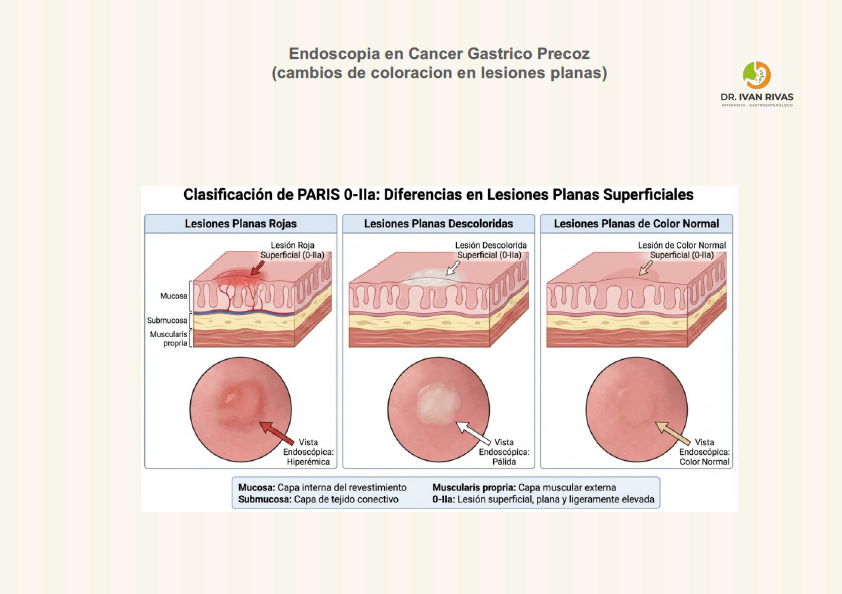
Lesiones elevadas: Color
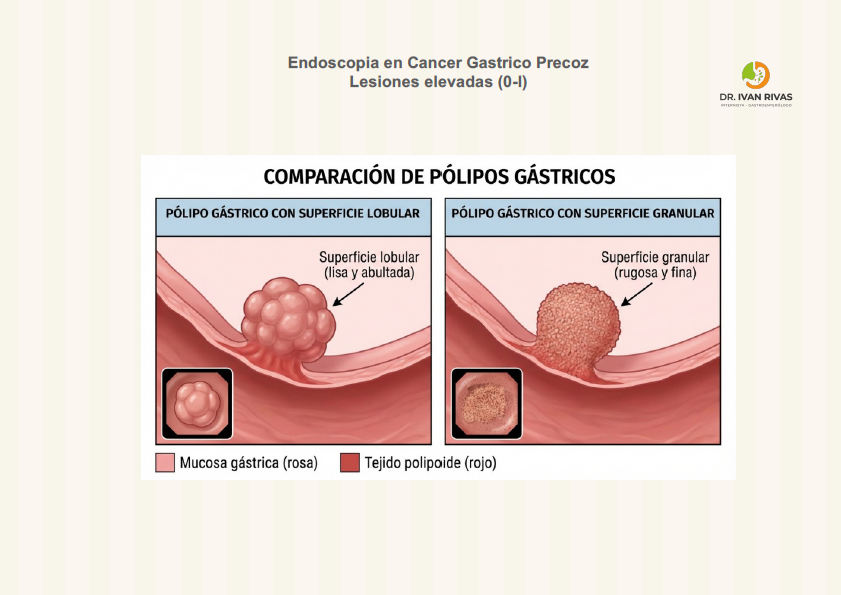
Características de la superficie de la lesión
Clasificación de Paris: lesiones planas
Clasificación de Paris: lesiones excavadas
Clasificaciones basadas en Narrow Band Imaging (NBI)
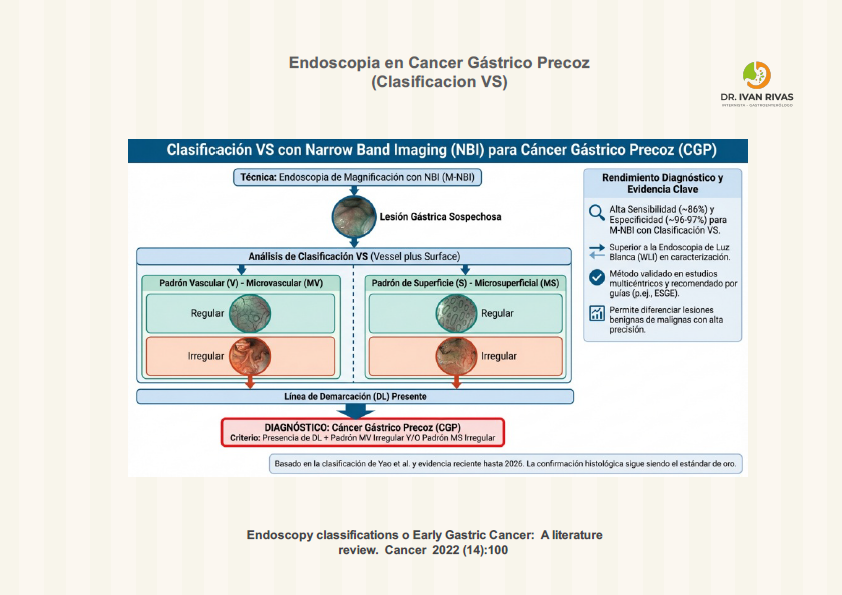
Clasificacion VS
- La clasificación endoscópica en el cáncer gástrico precoz ha evolucionado significativamente con la introducción de la imagen de banda estrecha (NBI, por sus siglas en inglés) frente a la endoscopia estándar con luz blanca (WLI)
- El NBI, especialmente cuando se utiliza con magnificación (ME-NBI), permite una evaluación detallada de los patrones microvasculares y de la superficie mucosa, lo que ha llevado al desarrollo de sistemas de clasificación específicos para la detección y caracterización de lesiones tempranas
- En la práctica clínica, la clasificación VS (vessel plus surface) propuesta por Yao et al. y la MESDA-G (Magnifying Endoscopy Simple Diagnostic Algorithm for Early Gastric Cancer) son algoritmos ampliamente utilizados para la evaluación de lesiones sospechosas mediante ME-NBI. Estos sistemas permiten diferenciar entre patrones vasculares y de superficie asociados a adenocarcinomas diferenciados y no diferenciados, mejorando la precisión diagnóstica y la predicción del subtipo histológico
- En comparación, la endoscopía estándar con luz blanca (WLI) carece de la capacidad para visualizar con detalle los patrones microvasculares y de superficie, lo que limita su sensibilidad y especificidad en la detección de cáncer gástrico precoz
- Estudios comparativos han demostrado que ME-NBI ofrece una sensibilidad y especificidad superiores para el diagnóstico de cáncer gástrico precoz (sensibilidad 86%, especificidad 96%), mientras que WLI presenta valores inferiores (sensibilidad 57%, especificidad 79%)
- Además, la identificación de la línea de demarcación de la lesión, crucial para la planificación de la resección endoscópica, es más precisa con NBI que con WLI, incluso sin magnificación
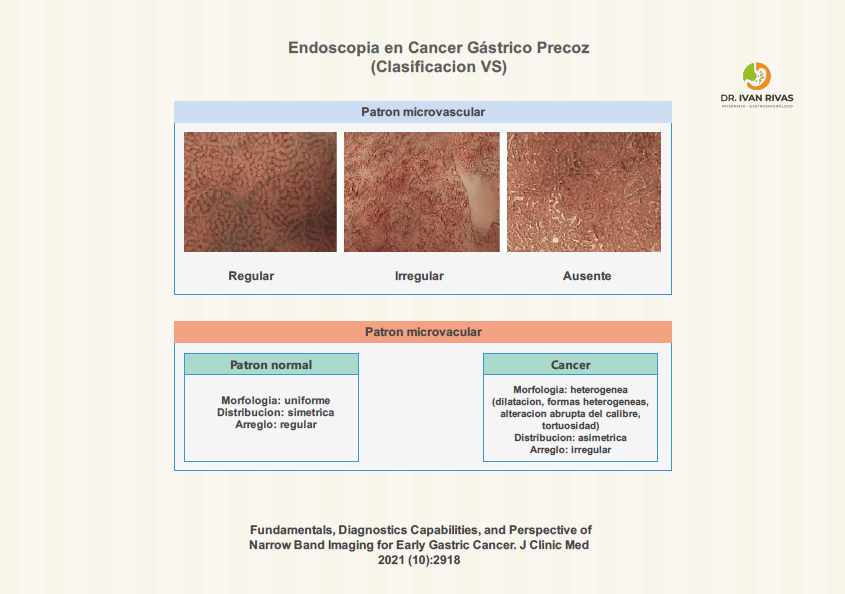
Patrón vascular
- El patrón vascular observado mediante narrow band imaging (NBI) en el cáncer gástrico precoz se caracteriza principalmente por la presencia de microvasculatura irregular, que puede adoptar diferentes morfologías según el subtipo histológico del tumor
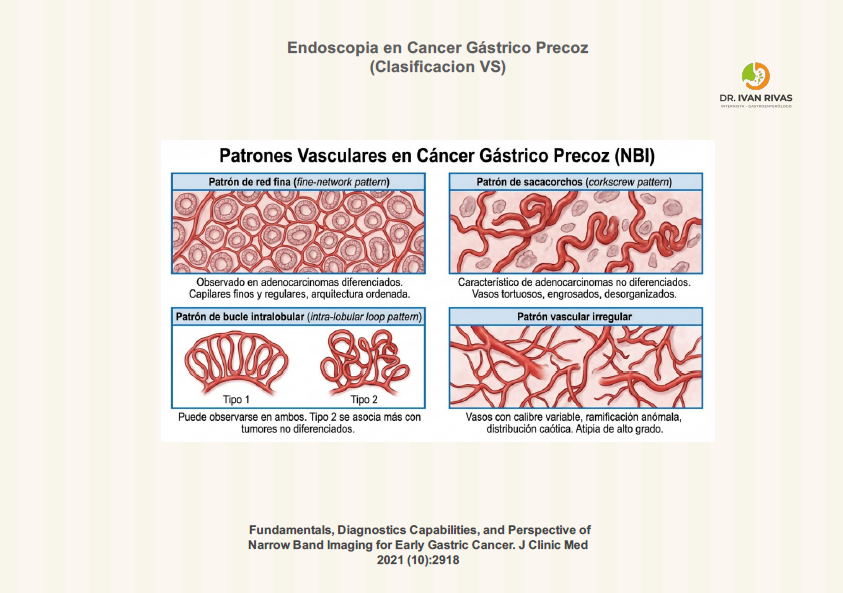
Los patrones más reconocidos y validados en la literatura incluyen:
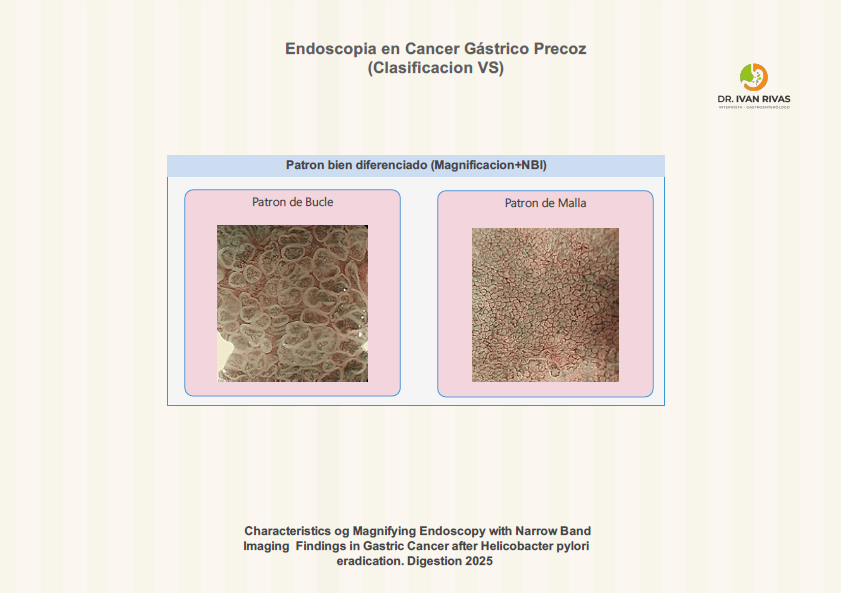
- Patrón de red fina (fine-network pattern): Este patrón se observa predominantemente en adenocarcinomas diferenciados y consiste en una red de capilares finos y regulares que rodean las glándulas, con una arquitectura vascular relativamente ordenada
- Patrón de sacacorchos (corkscrew pattern): Este patrón es característico de adenocarcinomas no diferenciados y se manifiesta como vasos tortuosos, engrosados y desorganizados, sin una disposición regular alrededor de las glándulas. La presencia de este patrón se asocia con una mayor probabilidad de histología no diferenciada
- Patrón de bucle intralobular (intralobular loop pattern): Se subdivide en tipo 1 y tipo 2, y puede observarse tanto en adenocarcinomas diferenciados como no diferenciados, aunque el tipo 2 se asocia más frecuentemente con tumores no diferenciados
- Patrón vascular irregular: La presencia de vasos con calibre variable, ramificación anómala y distribución caótica es un hallazgo fundamental para el diagnóstico de cáncer gástrico precoz mediante NBI, y se correlaciona con la presencia de atipia citológica y arquitectónica de alto grado
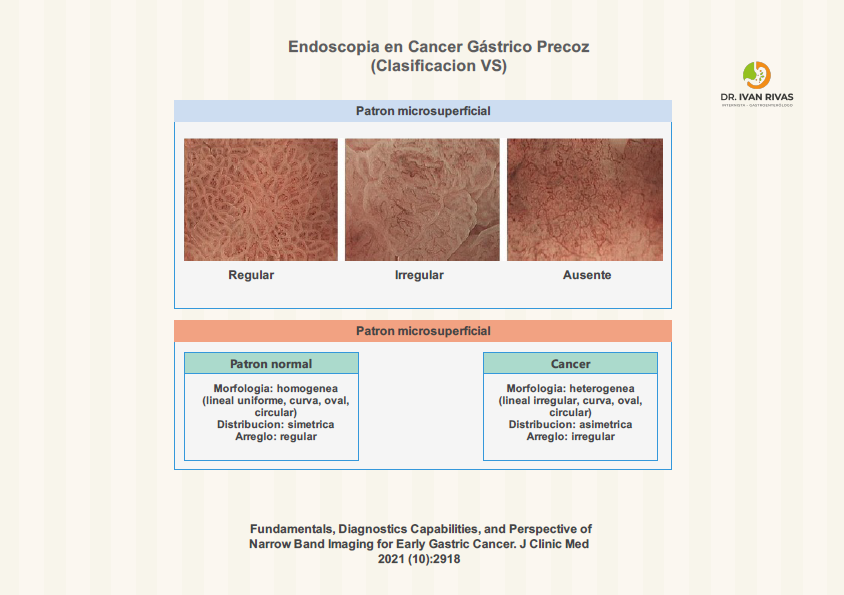
Patrón de Superficie
El patrón de superficie característico del cáncer gástrico precoz observado con Narrow Band Imaging (NBI), especialmente con magnificación, se define por la presencia de irregularidades en la arquitectura superficial de la mucosa. Los hallazgos más relevantes incluyen:
- Patrón micro superficial irregular: Se observa una pérdida de la disposición regular de las criptas o glándulas, con distorsión, desaparición o irregularidad de los orificios glandulares y de la estructura superficial. Este patrón se asocia directamente con atipia arquitectónica y citológica de alto grado, y es un marcador robusto de neoplasia intramucosa
- Ausencia de patrón superficial: En algunos casos, especialmente en carcinomas de células en anillo de sello o tumores poco diferenciados, puede haber una pérdida completa del patrón superficial, lo que se traduce en áreas donde no se identifican glándulas ni criptas, y la mucosa aparece homogénea o lisa bajo NBI con magnificación
- Cambios de coloración: El “pink pattern” descrito en la literatura reciente se refiere a una coloración rosada en la superficie mucosa, que se correlaciona con un aumento en la relación núcleo-citoplasma de las células neoplásicas y es útil para la identificación de adenocarcinomas diferenciados en estadios tempranos
- Bordes bien definidos: Las lesiones neoplásicas suelen presentar una delimitación clara respecto a la mucosa adyacente, lo que facilita la identificación de los márgenes de la lesión
En conjunto, la presencia de un patrón microsuperficial irregular o ausente, junto con cambios de coloración y bordes bien definidos, constituye el hallazgo endoscópico más característico del cáncer gástrico precoz bajo NBI. Estos criterios permiten una diferenciación precisa entre lesiones benignas y malignas, y se correlacionan estrechamente con la histopatología
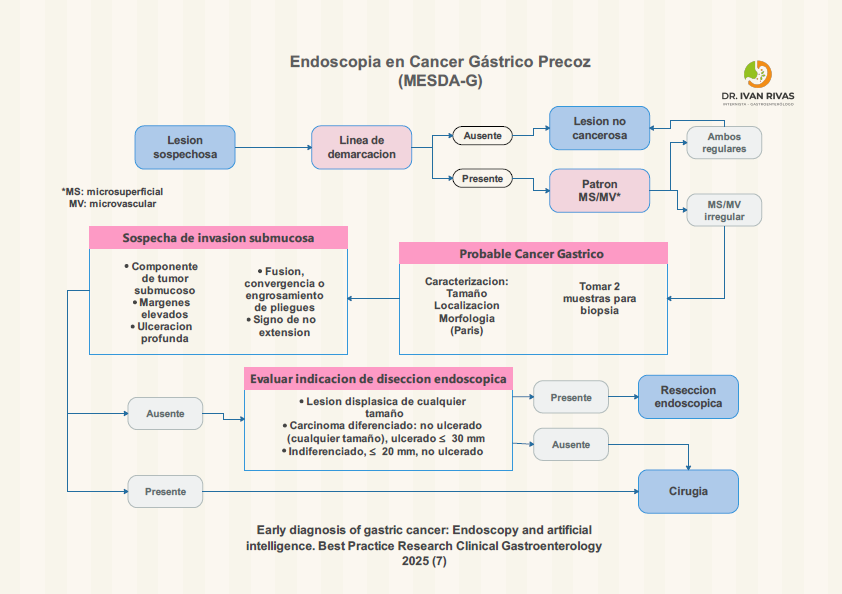
MESDA-G
- La técnica MESDA-G (Magnifying Endoscopy Simple Diagnostic Algorithm for Early Gastric Cancer) es un algoritmo diagnóstico desarrollado para la detección y caracterización del cáncer gástrico precoz mediante endoscopia con magnificación y narrow band imaging (NBI)
- Su utilidad radica en sistematizar la evaluación endoscópica de lesiones sospechosas, permitiendo distinguir de manera precisa entre lesiones benignas y malignas en la mucosa gástrica
- El algoritmo se basa en la observación de dos elementos clave: el patrón vascular y el patrón de superficie
- Cuando se identifica una zona con un borde claro, el algoritmo indica evaluar la microvasculatura y la microsuperficie; la presencia de irregularidad en cualquiera de estos patrones es altamente sugestiva de cáncer gástrico precoz
- MESDA-G ha demostrado mejorar la precisión diagnóstica respecto a la endoscopia convencional, facilitando la toma de decisiones sobre biopsia dirigida y delimitación de los márgenes de resección endoscópica
- En el contexto terapéutico, su aplicación permite seleccionar adecuadamente pacientes candidatos a resección endoscópica curativa, como la disección endoscópica submucosa (ESD), optimizando los resultados oncológicos y preservando la función gástrica
Tratamiento endoscópico
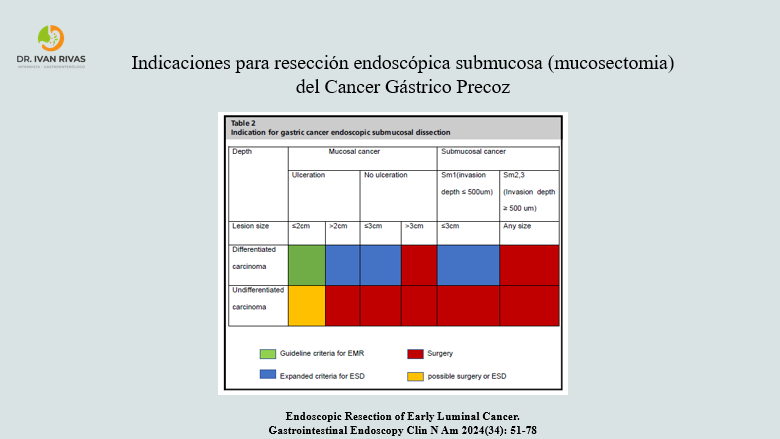
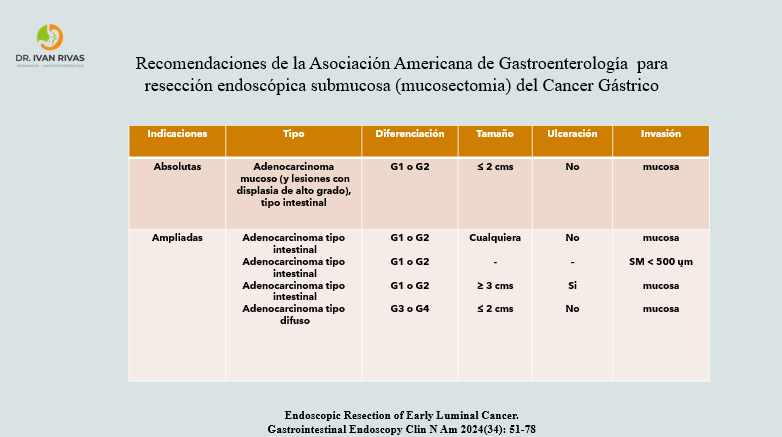
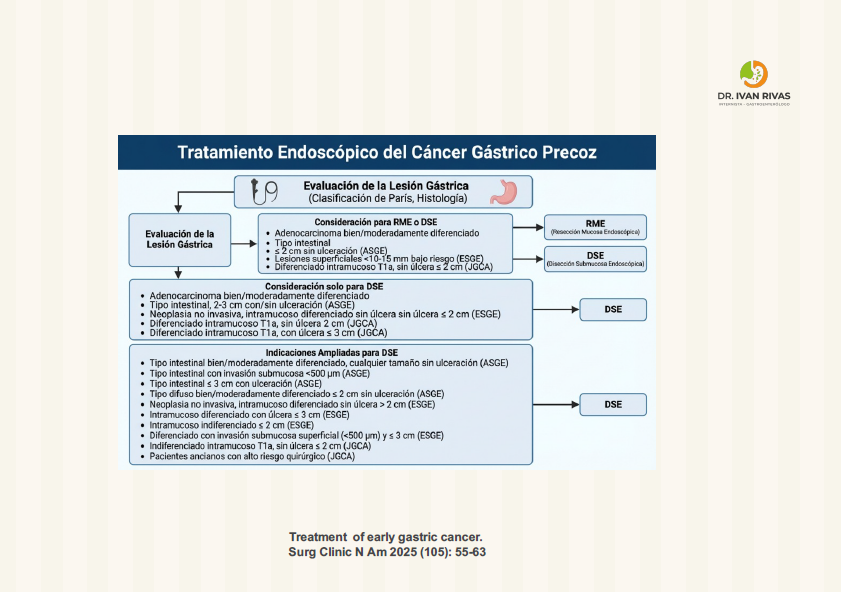
Indicaciones mucosectomía en Cáncer Gástrico Precoz
- las indicaciones de la disección mucosal endoscópica (DME) se basan en el riesgo de metástasis ganglionar y en la posibilidad de obtener una resección completa
- Se recomienda la DME como tratamiento de elección para la mayoría de lesiones gástricas superficiales
- Los criterios tienen un componente subjetivo. Por ejemplo es difícil distinguir endoscópicamente entre un cáncer limitado a la mucosa de un cáncer que comprometa la submucosa
- A pesar de que ultrasonido endoscópico puede ayudar en la determinación de la profundidad de la lesión antes de cualquier procedimiento tiene limitaciones en el caso de invasión submucosa muy pequeña, por lo tanto no representa un requisito previo a estos procedimientos
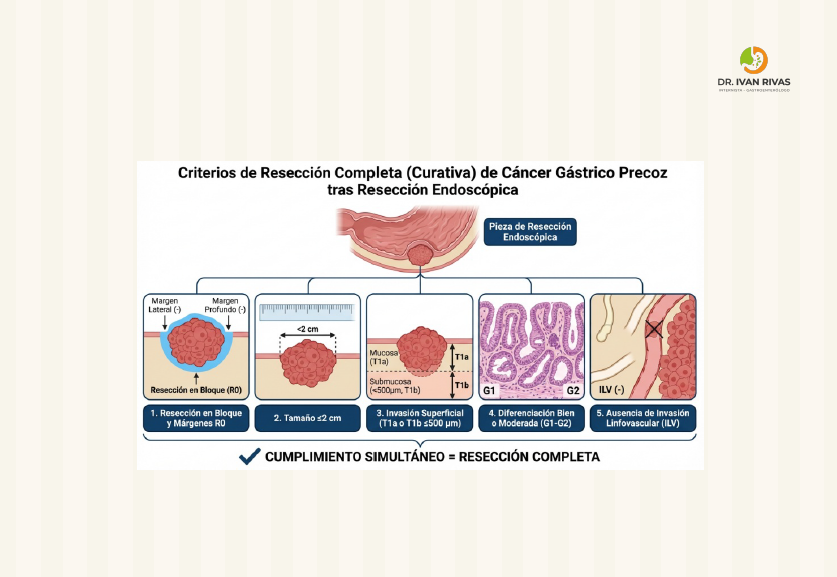
- La DME tiene indicaciones absolutas como es el caso de adenocarcinoma gástrico intramucoso (cT1a) con histología diferenciada, lesiones menores o iguales a 2 cms, sin evidencia de ulceración y sin invasión linfovascular
- Las indicaciones ampliadas de la DME incluyen lesiones de mayor tamaño, con histología no diferenciada e invasión submucosa mayor a 500 um con factores pronósticos favorables
- Las indicaciones pueden variar en las distintas instituciones y paises
- Factores del paciente como la edad y presencia de comorbilidades influyen en las decisiones terapéuticas a tomar